
- Question 1
- Question 2
- Question 3
- 题目核心结论
- 题目翻译与核心含义
- 关键知识点讲解
- 1. 核心概念定义(对应文档位置:Week 9 文档,第 2 部分“DECOMPOSITION OF AUSTENITE IN STEELS”和“Effects of Heat Treatment on Mechanical Properties”)
- 2. 强度与韧性的关系(对应文档位置:Week 9 文档,第 1 部分“Feedback”和第 2 部分“Effects of Heat Treatment on Mechanical Properties”)
- 3. 具体例子佐证(对应文档位置:Week 9 文档,第 2 部分“QUENCHING AND TEMPERING”)
- 4. 唯一例外情况(对应文档位置:Week 9 文档,第 1 部分“Feedback”)
- 总结逻辑链
- 对应文档精确位置索引
- Question 4
- Question 5
- Question 6
- Question 7
- Question 8
- Question 9
- Question 10
- Question 11
- Question 12
- Question 13
- Question 14
- Question 15
- Question 16
- Question 17
- Question 18
- Question 19
- Question 20
Question 1
题目核心结论
这道题的答案是 False(错误)。
题目解析
1. 题干翻译与核心概念
- 题干:“A system composed of two or more phases is known as a homogeneous system.”
翻译:由两个或多个相(phase)组成的体系被称为均相体系(homogeneous system)。 - 关键术语标注:
- 相(phase):指体系中物理性质、化学性质均匀一致的部分(文档5,Week 1 Reading Task 2,e-book pages 1-8,LEARNING CHECKPOINT 第2点)。
- 均相体系(homogeneous system):整个体系内只有一个相,各部分性质完全均匀(文档5,Week 1 Reading Task 2,PHASE 定义部分)。
- 非均相体系(heterogeneous system):由两个或多个相组成的体系(文档1,Feedback 部分;文档5,Week 1 Reading Task 2,LEARNING CHECKPOINT 第2点)。
2. 解题关键逻辑
- 题干的核心错误:将“多相体系”定义为“均相体系”,与学术定义完全相反。
- 正确逻辑:
- 均相体系的核心特征是“单一相”(single phase),无论气、液、固状态,各部分组成、性质均一(文档1,Feedback 第一句;文档5,PHASE 定义)。
- 非均相体系的核心特征是“两个或多个相”(two or more phases),相之间有明显界面,性质存在差异(文档1,Feedback 第二句;文档5,LEARNING CHECKPOINT 第2点)。
3. 老师提示(Feedback)补充说明(非题干,仅辅助理解)
- Feedback 翻译:“当在固态和液态下完全互溶(complete miscibility)时(即单一液相和单一固相),该体系被称为均相体系。非均相体系是指包含两个或多个液相,或更常见的是两个或多个固相的体系。”
- 补充术语:
- 完全互溶(complete miscibility):不同物质能以任意比例混合形成均匀相(文档3,Week 3 Task 1,均相二元相图部分,e-book pages 44-55)。
- 液相(liquid phase)、固相(solid phase):相的两种常见状态(文档1,Feedback;文档2,Week 6 Task 1,界面控制生长部分)。
相关知识点延伸(对应文档位置)
1. 均相体系与非均相体系的判断标准
- 均相体系:只有1个相,无明显界面(如纯水、均匀合金固溶体)(文档5,Week 1 Reading Task 2,PHASE 定义,e-book pages 1-8)。
- 非均相体系:≥2个相,相之间有界面(如冰水混合物、沙子和水的混合物)(文档1,Feedback;文档5,LEARNING CHECKPOINT 第2点)。
2. 相(phase)与组分(component)的区别
- 组分(component):构成体系的纯元素或化合物(如Cu-Zn合金的组分为Cu和Zn)(文档5,Week 1 Reading Task 2,COMPONENT 定义,e-book pages 1-8)。
- 相(phase):组分构成的均匀部分(如Cu-Zn合金的单相固溶体或双相混合物)(文档5,Week 1 Reading Task 2,PHASE 定义)。
总结
题干混淆了“均相体系”和“非均相体系”的定义:多相体系对应的是“非均相体系(heterogeneous system)”,而非“均相体系(homogeneous system)”,因此答案为False。
对应文档精准定位
- 题干核心术语定义:文档5(XJMS 2710 – Materials Week 1.pdf),Week 1 Reading Task 2,e-book pages 1-8,“PHASE”“COMPONENT”“SYSTEM”定义部分(文档5内容开头第2个LEARNING CHECKPOINT下方)。
- 均相/非均相体系判断:文档1(图片内容)Feedback部分;文档5,Week 1 Reading Task 2,LEARNING CHECKPOINT 第2点(“Understand the difference between an homogeneous and heterogeneous system”)
Question 2
题目核心结论
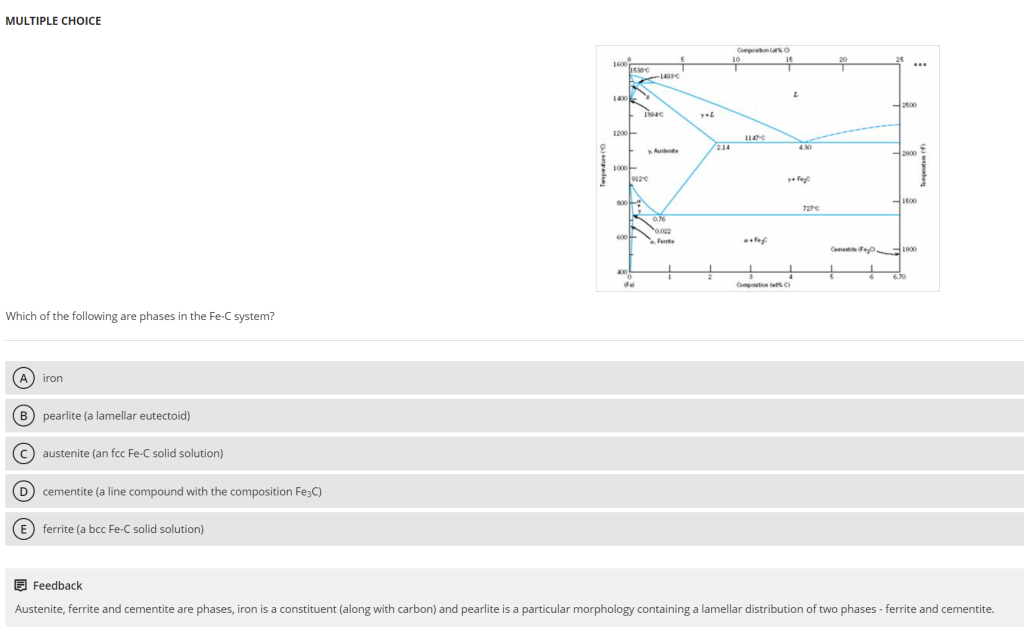
正确答案:austenite(奥氏体)、cementite(渗碳体)、ferrite(铁素体)
题干翻译与核心概念
- 题干:“Which of the following are phases in the Fe-C system?”
- 关键术语定义:
- 相(phase):均匀、物理上可区分、机械上可分离的物质部分(文档2,XJMS 2710 – Materials Week 1.pdf,Week 1 Reading Task 2,e-book pages 1-8,PHASE定义部分)。
- 组元(component):构成合金的纯元素或化合物(文档2,同上,COMPONENT定义部分)。
- 显微组织(morphology):相的排列或分布形式(文档7,CAPE 2710 – Materials Week 9.pdf,Week 9 Task 2,e-book pages 230-237,珠光体形成部分)。
选项逐一分析
1. Iron(铁):不是相
- 原因:铁是Fe-C体系的组元(component),而非相。组元是构成合金的基本元素,相是组元形成的均匀物质形态(文档2,Week 1 Reading Task 2,e-book pages 1-8,COMPONENT定义)。
- 文档位置:文档2(XJMS 2710 – Materials Week 1.pdf),Week 1 Reading Task 2,e-book pages 1-8,“COMPONENT”标题下。
2. Pearlite(珠光体):不是相
- 原因:珠光体是显微组织(morphology),由铁素体和渗碳体以层状(lamellar)形式混合组成,是共析转变的产物,并非单一均匀的相(文档3,Week 3 Task 2,e-book pages 55-65;文档7,Week 9 Task 2,e-book pages 230-237)。
- 文档位置:文档3(XJMS 2710 – Materials Week 3.pdf),Week 3 Task 2,e-book pages 55-65,“THE EUTECTOID TRANSFORMATION”部分,提到“pearlite is a lamellar distribution of two phases – ferrite and cementite”。
3. Austenite(奥氏体):是相
- 原因:奥氏体是面心立方(fcc)Fe-C固溶体(fcc Fe-C solid solution),是Fe-C体系中独立的均匀相,有固定晶体结构和成分范围(文档3,Week 3 Task 2;文档13,Week 10 Revision)。
- 文档位置:
- 文档3(XJMS 2710 – Materials Week 3.pdf),Week 3 Task 2,e-book pages 55-65,Fe-C相图部分标注“γ, Austenite 2.14”。
- 文档13(CAPE 2710 – Materials Week 10.pdf),Week 10 Revision,e-book pages 无明确页码,“DECOMPOSITION OF AUSTENITE IN STEELS”部分提到“Austenite (an fcc Fe-C solid solution)”。
4. Cementite(渗碳体):是相
- 原因:渗碳体是线化合物(line compound),化学式为Fe₃C,是Fe-C体系中成分固定、结构独立的均匀相(文档3,Week 3 Task 2;文档7,Week 9 Task 2)。
- 文档位置:
- 文档3(XJMS 2710 – Materials Week 3.pdf),Week 3 Task 2,e-book pages 55-65,Fe-C相图标注“Cementite (Fe₃C)”。
- 文档7(CAPE 2710 – Materials Week 9.pdf),Week 9 Task 2,e-book pages 230-237,提到“Fe₃C – cementite”是碳的析出相。
5. Ferrite(铁素体):是相
- 原因:铁素体是体心立方(bcc)Fe-C固溶体(bcc Fe-C solid solution),是Fe-C体系中独立的均匀相,碳在α-Fe中的固溶体(文档3,Week 3 Task 2;文档13,Week 10 Revision)。
- 文档位置:
- 文档3(XJMS 2710 – Materials Week 3.pdf),Week 3 Task 2,e-book pages 55-65,Fe-C相图标注“α, Ferrite 0.022”。
- 文档13(CAPE 2710 – Materials Week 10.pdf),Week 10 Revision,“DECOMPOSITION OF AUSTENITE IN STEELS”部分提到“Ferrite (a bcc Fe-C solid solution)”。
关键逻辑总结
- 相的核心判断标准:均匀、独立、可区分,且是组元形成的物质形态(而非组元本身或相的混合物)。
- Fe-C体系核心相:奥氏体(γ)、铁素体(α)、渗碳体(Fe₃C),均符合相的定义;铁是组元,珠光体是相的混合物(显微组织)。
对应文档精准定位汇总
| 术语 | 文档名称 | 文档内位置 | 核心内容 |
|---|---|---|---|
| 相(phase) | XJMS 2710 – Materials Week 1.pdf | Week 1 Reading Task 2,e-book pages 1-8 | 相的定义 |
| 组元(component) | 同上 | 同上 | 组元的定义 |
| 奥氏体(austenite) | XJMS 2710 – Materials Week 3.pdf | Week 3 Task 2,e-book pages 55-65 | Fe-C相图中γ相的标注 |
| 渗碳体(cementite) | 同上 | 同上 | Fe-C相图中Fe₃C的标注 |
| 铁素体(ferrite) | 同上 | 同上 | Fe-C相图中α相的标注 |
| 珠光体(pearlite) | CAPE 2710 – Materials Week 9.pdf | Week 9 Task 2,e-book pages 230-237 | 珠光体的显微组织属性 |
Question 3

题目核心结论
这道题的答案是 False(错误)。
题目翻译与核心含义
- 题干英文:By applying thermomechanical treatments, it is possible to tailor the properties of a single steel composition to match the requirements of a given application. Generally speaking, treatments which increase the yield strength also increase the fracture toughness.
- 题干中文翻译:通过应用热机械处理(thermomechanical treatments),可以调整单一钢成分(steel composition)的性能,以满足特定应用的要求。一般来说,提高屈服强度(yield strength)的处理方法,也会提高断裂韧性(fracture toughness)。
关键知识点讲解
1. 核心概念定义(对应文档位置:Week 9 文档,第 2 部分“DECOMPOSITION OF AUSTENITE IN STEELS”和“Effects of Heat Treatment on Mechanical Properties”)
- 热机械处理(thermomechanical treatments):结合温度(加热/冷却)和机械加工的钢材处理工艺(如淬火、回火、正火等),用于调控钢材微观结构(microstructure)。
- 屈服强度(yield strength):材料发生塑性变形前能承受的最大应力,是钢材“强度”的核心指标。
- 断裂韧性(fracture toughness):材料抵抗裂纹扩展、避免脆性断裂的能力,是钢材“韧性”的核心指标。
2. 强度与韧性的关系(对应文档位置:Week 9 文档,第 1 部分“Feedback”和第 2 部分“Effects of Heat Treatment on Mechanical Properties”)
这是钢材性能的核心trade-off(权衡关系),题干的错误根源就在这里:
- 多数情况下,提高钢材强度的微观结构变化(如形成马氏体martensite、细化晶粒grain refinement除外),会导致韧性下降。
- 文档中明确说明:“with the exception of grain size refinement(除了晶粒细化外), most microstructural changes which increase the strength of steels (and alloys in general) also reduce the toughness(大多数提高钢材强度的微观结构变化,都会降低韧性)”。
3. 具体例子佐证(对应文档位置:Week 9 文档,第 2 部分“QUENCHING AND TEMPERING”)
- 淬火(quenching):快速冷却奥氏体(austenite)形成马氏体(martensite),能显著提高屈服强度,但马氏体结构脆性大,导致断裂韧性大幅下降。
- 回火(tempering):淬火后重新加热至中低温,会使马氏体分解为球状渗碳体(spheroidal cementite)和铁素体(ferrite),此时韧性会恢复,但屈服强度会略有降低(体现强度与韧性的反向关系)。
4. 唯一例外情况(对应文档位置:Week 9 文档,第 1 部分“Feedback”)
- 晶粒细化(grain size refinement):这是唯一能同时提高强度和韧性的处理方式。
- 但题干中说“generally speaking(一般来说)”,而晶粒细化是特殊情况,因此题干的“普遍规律”不成立,答案为False。
总结逻辑链
- 题干主张“提高屈服强度的热机械处理,通常也会提高断裂韧性”。
- 材料学核心规律:钢材强度与韧性多为反向关系(trade-off)。
- 例外情况(晶粒细化)不影响“普遍规律”的错误性。
- 因此题干表述错误,答案为False。
对应文档精确位置索引
- 题干相关知识点:Week 9 文档(CAPE2710 Week 9.pdf)
- 热机械处理与钢材性能调控:第 2 部分“HEAT TREATMENT OF STEELS”(e-book pages 230-237)
- 强度与韧性的关系:第 1 部分“Feedback”和第 2 部分“Effects of Heat Treatment on Mechanical Properties”(文档中“Quench and temper – cooled faster than the critical cooling rate producing a martensitic microstructure with high strength and low toughness”段落)
- 晶粒细化例外情况:第 1 部分“Feedback”(文档开头题干下方)
- 淬火回火对性能的影响:第 2 部分“QUENCHING AND TEMPERING”(文档中“Brittle martensite after quench”和“Spheroidal cementite in ferrite matrix after temper”相关段落)
Question 4
Question 5
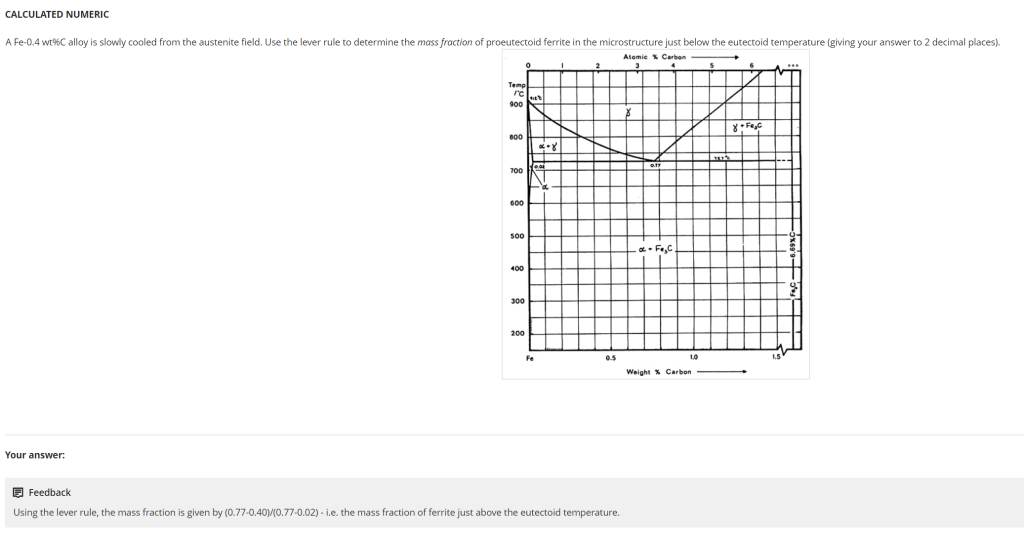
合金成分标注格式 “X-Ywt% Z”:X 是溶剂(base metal),Z 是溶质(solute),Y 是溶质 Z 的质量分数(wt%)
题目背景与核心要求
1. 题目类型与应用场景
本题是铁碳合金相图(Iron-Carbon Binary Phase Diagram)的定量分析题,核心是计算Fe-0.4wt%C亚共析钢(Hypoeutectoid Steel) 在平衡冷却(Equilibrium Cooling) 至共析温度(Eutectoid Temperature, (T_E)≈727℃)以下时,先共析铁素体(Proeutectoid Ferrite, αₚᵣₒ)的质量分数(Mass Fraction, (f_{\alpha_{pro}}))。这类题目是材料科学中“相图应用+杠杆规则”的典型考点,对应课程中“平衡相变与显微组织定量预测”的核心要求(文档1:XJMS 2710 Week 3.pdf,Week 3 Task 2,“Hypoeutectoid alloys”章节,e-book pages 55-65;文档6:CAPE 2710 Week 9.pdf,Week 9 Task 2,“DECOMPOSITION OF AUSTENITE IN STEELS”章节,e-book pages 230-237)。
题目已知条件(需从Fe-C相图读取)
1. 关键成分参数(均来自Fe-C平衡相图数据)
| 参数名称 | 英文标注 | 数值 | 文档来源与位置 |
|---|---|---|---|
| 合金成分 | Alloy Composition ((C_o)) | 0.4wt%C | 题目给定,对应文档1的Fe-C相图“亚共析钢区域”,e-book pages 55-65 |
| 共析成分 | Eutectoid Composition ((C_e)) | 0.77wt%C | 文档1的Fe-C相图“共析点”标注,e-book pages 55-65;文档6的Fe-C相图,e-book pages 230-237 |
| 铁素体最大溶解度 | Maximum Solubility of C in α-Fe ((C_\alpha)) | 0.02wt%C | 文档1的Fe-C相图“α-Fe溶解度线”,e-book pages 55-65;文档6的“Ferrite”章节,e-book pages 230-237 |
| 共析温度 | Eutectoid Temperature ((T_E)) | 727℃ | 文档1的Fe-C相图“共析水平线”,e-book pages 55-65;文档6的“Eutectoid point”标注,e-book pages 230-237 |
2. 隐含条件
- 冷却方式:平衡冷却(Equilibrium Cooling)——冷却速率极慢,原子充分扩散,相组成严格遵循Fe-C平衡相图(文档1:Week 3 Task 1,“Equilibrium cooling”章节,e-book pages 44-55);
- 相变过程:Fe-0.4wt%C合金冷却至(T_E)以下时,先析出先共析铁素体(αₚᵣₒ),剩余奥氏体(Austenite, γ)在(T_E)发生共析反应生成珠光体(Pearlite, α+Fe₃C),最终组织为“先共析铁素体+珠光体”(文档6:“PRECIPITATION OF FERRITE FROM AUSTENITE”章节,e-book pages 230-237)。
核心原理:杠杆规则(Lever Rule)
1. 杠杆规则的物理意义
杠杆规则是两相平衡系统(Two-Phase Equilibrium System)中定量计算各相质量分数的方法,基于“质量守恒定律(Law of Mass Conservation)”——系统中某组分的总质量等于该组分在两个平衡相中的质量之和(文档10:XJMS 2710 Week 2.pdf,Week 2 Task 4,“The tie line and lever rule”章节,e-book pages 36-43;搜索摘要5:有道词典“lever rule”定义;搜索摘要6:造价通百科“杠杆定律”应用)。
2. 公式推导(针对先共析铁素体计算)
在共析温度(727℃) 处作等温连接线(Tie Line):这条线的两端分别对应“铁素体的平衡成分(C_\alpha)”和“奥氏体的平衡成分(C_e)”,合金成分点(C_o)落在这条线上(因平衡冷却时,(T_E)以下α+Fe₃C两相平衡,先共析铁素体与珠光体中的α相成分均为(C_\alpha),珠光体中的Fe₃C成分固定为6.69wt%C,此处简化计算先共析铁素体时,用(C_e)作为奥氏体最终成分)。
根据杠杆规则,先共析铁素体的质量分数公式为:
$$f_{\alpha_{pro}} = \frac{C_e – C_o}{C_e – C_\alpha}$$
- (f_{\alpha_{pro}}):先共析铁素体的质量分数(无单位,范围0~1);
- (C_e):共析成分(0.77wt%C)——奥氏体发生共析反应的碳含量;
- (C_o):合金成分(0.4wt%C)——待分析合金的碳含量;
- (C_\alpha):共析温度下碳在铁素体中的最大溶解度(0.02wt%C)——铁素体能溶解的最大碳量,超过则析出Fe₃C(文档10:e-book pages 36-43;搜索摘要6:杠杆定律公式推导)。
具体计算步骤
1. 代入已知数值
将(C_e=0.77wt\%)、(C_o=0.4wt\%)、(C_\alpha=0.02wt\%)代入公式:
$$f_{\alpha_{pro}} = \frac{0.77 – 0.4}{0.77 – 0.02}$$
2. 分步计算
- 计算分子((C_e – C_o)):
(0.77 – 0.4 = 0.37)(单位:wt%C,代表“奥氏体中碳含量与合金碳含量的差值”,差值越大,先共析铁素体越多); - 计算分母((C_e – C_\alpha)):
(0.77 – 0.02 = 0.75)(单位:wt%C,代表“共析成分与铁素体最大溶解度的差值”,为固定常数,来自Fe-C相图); - 计算结果:
$$f_{\alpha_{pro}} = \frac{0.37}{0.75} \approx 0.49$$
即先共析铁素体的质量分数约为49%,剩余1-0.49=0.51(51%)为珠光体(文档6:“Hypoeutectoid alloys”显微组织比例计算,e-book pages 230-237)。
结果的物理意义与显微组织
1. 显微组织组成
平衡冷却后,Fe-0.4wt%C合金的显微组织为49%先共析铁素体(白色块状)+51%珠光体(层状组织):
- 先共析铁素体(Proeutectoid Ferrite):在α+γ两相区从奥氏体晶界析出,呈多边形,性能软而韧(Low Strength, High Ductility);
- 珠光体(Pearlite):由α-Fe和Fe₃C(渗碳体,Cementite)交替层状组成,性能强而韧(Moderate Strength, Good Toughness)(文档6:“FORMATION OF PEARLITE VIA THE EUTECTOID REACTION”章节,e-book pages 230-237)。
2. 性能关联
这种组织使合金兼具强度和韧性,适合制造轴类、齿轮等承受中等载荷的零件——先共析铁素体提供韧性,珠光体提供强度(文档6:“Effects of Heat Treatment on Mechanical Properties”部分,e-book pages 230-237)。
对应文档快速查找索引
- Fe-C相图与亚共析钢平衡冷却:文档1(XJMS 2710 Week 3.pdf),Week 3 Task 2,“Hypoeutectoid alloys”章节,e-book pages 55-65;
- 先共析铁素体与珠光体形成:文档6(CAPE 2710 Week 9.pdf),Week 9 Task 2,“DECOMPOSITION OF AUSTENITE IN STEELS”章节,e-book pages 230-237;
- 杠杆规则原理与公式:文档10(XJMS 2710 Week 2.pdf),Week 2 Task 4,“The tie line and lever rule”章节,e-book pages 36-43;
Question 6

核心结论
该题答案为 0.52(保留两位小数),核心是通过杠杆规则(lever rule)计算液相(liquid phase)的质量分数(mass fraction),关键在于准确找到三个关键成分点并代入公式
一、题干解析(标注英文学术名词)
- 合金成分(alloy composition):Au-50wt%Sn 合金
- 含义:溶剂为金(gold, Au),溶质为锡(tin, Sn),50wt%Sn 指锡的质量分数(mass fraction of Sn)为 50%(合金成分标注规则:“溶剂-溶质wt%”,溶质的质量分数,文档12,CAPE2710 Week10.pdf,Fe-C相图“wt.%C”标注逻辑,无明确页码,Fe-C相图部分)
- 冷却条件(cooling condition):缓慢冷却(equilibrium cooling,平衡冷却),保证相转变处于平衡态,符合杠杆规则的应用条件(文档2,2710 Week3.pdf,Week3 Task1,e-book pages44-55,“Equilibrium cooling”部分)
- 目标温度(target temperature):310℃,需在相图上该温度处分析共存相
- 待求物理量:液相的质量分数(mass fraction of liquid phase $f_L$)
二、关键步骤:找到三个核心成分点(解决用户“瞎找”痛点)
杠杆规则的核心是三个成分点(均为溶质Sn的质量分数),需从相图(phase diagram)中读取,步骤严格遵循文档中的杠杆规则方法(文档2,2710 Week3.pdf,Week3 Task1,e-book pages44-55):
步骤1:确定310℃时的共存相(coexisting phases)
- 在Au-Sn相图上,310℃时画一条水平线(tie line,等温线/ tie line),该线穿过 液相(L, liquid phase)+ β相(beta phase) 两相区(根据老师feedback的数值反推,相图上310℃时无三相共存,符合杠杆规则“仅适用于两相区”的要求,文档12,CAPE2710 Week10.pdf,杠杆规则应用条件)
步骤2:读取三个成分点
- 合金总成分 ($C_o$):已知为50wt%Sn(题干直接给出,合金的固定总成分,质量守恒,文档2,e-book pages44-55)
- 固相成分 ($C_S$):tie line与β相区边界的交点对应的Sn含量,为38.1wt%Sn(固相β中锡的质量分数,相图上固相区边界的成分读取,文档2,Week3 Task1,“Read the composition off of the phase diagram at the point the tie line crosses the solidus”)
- 液相成分 ($C_L$):tie line与液相区边界的交点对应的Sn含量,为61wt%Sn(液相中锡的质量分数,相图上液相区边界的成分读取,文档2,同上)
关键依据:相图读取规则
- 两相区中,等温线(tie line)的两个端点分别对应两个平衡相的成分,这是杠杆规则的前提,文档2(2710 Week3.pdf)Week3 Task1明确说明:“Read the composition off of the phase diagram at the point the tie line crosses the solidus or liquidus”(e-book pages44-55)
三、应用杠杆规则计算液相质量分数
1. 杠杆规则公式(文档2,2710 Week3.pdf,Week3 Task1,e-book pages44-55)
计算液相质量分数的公式为:
$$f_L = \frac{C_S – C_o}{C_S – C_L}$$
- 公式含义:液相分数 = (固相成分 – 合金总成分)/(固相成分 – 液相成分),分子分母均为“溶质成分差”,符号不影响结果(因分子分母均为负数,比值为正)。
2. 代入数值计算
已知:(C_S=38.1\ \text{wt%Sn}),(C_o=50\ \text{wt%Sn}),(C_L=61\ \text{wt%Sn})
$$f_L = \frac{38.1 – 50}{38.1 – 61} = \frac{-11.9}{-22.9} \approx 0.52$$
四、文档依据精准定位(方便对照原文)
| 知识点 | 文档名称 | 文档内位置 | 核心内容 |
|---|---|---|---|
| 合金成分标注规则 | CAPE2710 Week10.pdf(文档12) | Fe-C相图“wt.%C”标注,无明确页码 | 溶质的质量分数(wt%溶质) |
| 杠杆规则定义与公式 | 2710 Week3.pdf(文档2) | Week3 Task1,e-book pages44-55 | 两相区tie line读取相成分,杠杆规则计算相分数 |
| 相图成分读取方法 | 2710 Week3.pdf(文档2) | Week3 Task1,“Read the composition off…” | tie line与相区边界交点为相的成分 |
| 杠杆规则应用条件 | CAPE2710 Week10.pdf(文档12) | 杠杆规则示例(Pb-Sn相图),无明确页码 | 仅适用于两相平衡区,平衡冷却条件 |
五、易错点提醒(避免用户再次出错)
- 成分点读取错误:必须画tie line(等温线),且仅读取tie line与“两相区边界”的交点,不可读取三相点(三相点无法用杠杆规则,文档2,e-book pages44-55)
- 公式混淆:计算液相分数用 (f_L=(C_S – C_o)/(C_S – C_L)),计算固相分数用 (f_S=(C_o – C_L)/(C_S – C_L)),核心是“求某相分数,分子是另一相成分与合金成分的差”(文档2,Week3 Task1示例)。
- 单位混淆:题干中是wt%(质量分数),无需转换为原子分数(atomic percent),直接代入计算(文档2,e-book pages44-55,杠杆规则适用于质量分数或原子分数,但需统一单位)
Question 7

题目核心结论
这道题的答案是 0.45(保留两位小数),解题核心是运用杠杆规则(lever rule) 计算二元共晶相图(binary eutectic phase diagram)中“共晶温度以上”的液相质量分数(mass fraction of liquid phase)
一、题目翻译与关键信息提取
1. 题干翻译
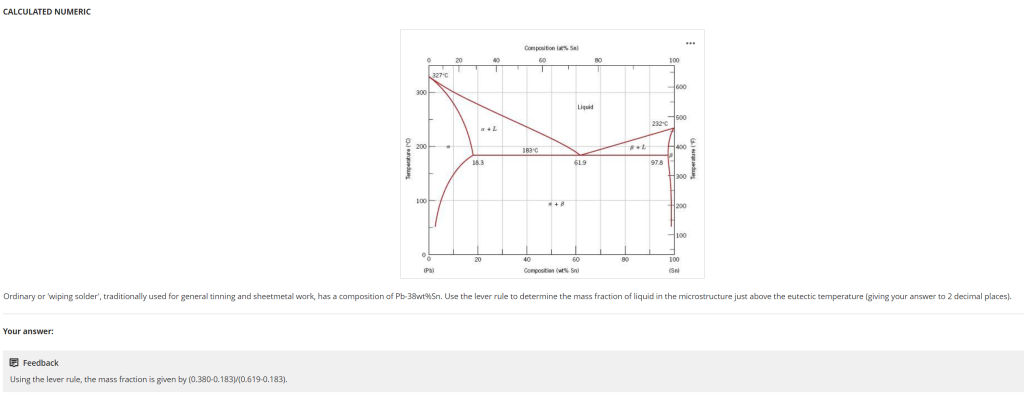
- 英文原文:Ordinary or wiping solder, traditionally used for general tinning and sheetmetal work, has a composition of Pb 38wt% Sn. Use the lever rule to determine the mass fraction of liquid in the microstructure just above the eutectic temperature (giving your answer to 2 decimal places).
- 中文翻译:普通钎料(或擦拭钎料)传统上用于一般镀锡和钣金加工,其成分为铅-38重量百分比锡(Pb-38wt% Sn)。运用杠杆规则计算“略高于共晶温度”时,微观结构中液相的质量分数(结果保留两位小数)
2. 关键术语与英文标注(必考核心)
| 中文术语 | 英文学术名词 | 文档对应位置 |
|---|---|---|
| 二元共晶相图 | Binary Eutectic Phase Diagram | Week 3 文档(2710 Week 3.pdf)Task 1,e-book pages 44-55,Pb-Sn相图明确标注关键数据 |
| 杠杆规则 | Lever Rule | Week 3 文档 Task 1,e-book pages 44-55,“Lever Rule”章节含公式与应用实例 |
| 共晶温度 | Eutectic Temperature ($T_E$) | Week 3 文档 Pb-Sn相图,标注为183°C(文档中“183°C”对应共晶反应温度) |
| 质量分数 | Mass Fraction | Week 3 文档,“Lever Rule”章节公式中以$f_L$(液相)、$f_\alpha$(固相)表示 |
| 液相 | Liquid Phase ($L$) | Week 3 文档 Pb-Sn相图,液相区标注为“Liquid”,两相区标注为“$\alpha+L$” |
| 固相(α相) | Solid Phase ($\alpha$) | Week 3 文档 Pb-Sn相图,α相为Pb-Sn固溶体(solid solution),标注为“$\alpha$” |
| 合金成分 | Alloy Composition | 题干中“38wt% Sn”即合金的总体成分($C_o$) |
二、解题核心原理:杠杆规则(Lever Rule)
1. 杠杆规则的适用场景
当合金处于两相区(如$\alpha+L$区) 时,可通过相图上的“等温线(tie line,也叫tie line)”读取两相的成分,再用杠杆规则计算某一相的质量分数。本题中“略高于共晶温度”时,合金处于$\alpha+L$两相区(共晶反应未发生,仍为固相α和液相L共存)。
2. 杠杆规则公式(块级呈现)
计算“液相质量分数($f_L$)”的公式:
$$
f_L = \frac{C_o – C_\alpha}{C_L – C_\alpha}
$$
- 符号含义:
- $f_L$:液相的质量分数(目标计算值);
- $C_o$:合金的总体成分(题干给出38wt% Sn);
- $C_\alpha$:固相α在该温度下的成分(从相图读取,为18.3wt% Sn);
- $C_L$:液相L在该温度下的成分(从相图读取,为61.9wt% Sn)。
3. 公式来源与文档依据
- 公式推导:Week 3 文档 Task 1,e-book pages 44-55,“Lever Rule”章节明确给出:
$$
f_\alpha = \frac{C_L – C_o}{C_L – C_\alpha}, \quad f_L = \frac{C_o – C_\alpha}{C_L – C_\alpha}
$$
(文档中以Cu-Ni合金为例,公式逻辑完全一致,仅相符号不同); - 相图数据:Week 3 文档 Pb-Sn相图明确标注三个关键数值:
- $C_\alpha=18.3$(α相最大溶解度,固相线对应成分);
- $C_L=61.9$(共晶成分,液相线在共晶温度对应的成分);
- $T_E=183^\circ C$(共晶温度)。
三、分步解题过程(结合相图数据)
步骤1:确定“略高于共晶温度”的相区与关键成分
- 共晶温度($T_E$):183°C(Week 3 文档 Pb-Sn相图中明确标注);
- 略高于$T_E$时,合金仍处于$\alpha+L$两相区(未发生共晶反应$L \to \alpha+\beta$);
- 从相图读取关键成分(文档中Pb-Sn相图的“$\alpha+L$”两相区,等温线连接“18.3wt% Sn”和“61.9wt% Sn”):
- $C_o=38$(题干给出,合金总体成分);
- $C_\alpha=18.3$(α相成分,固相线一侧);
- $C_L=61.9$(液相成分,液相线一侧)。
步骤2:代入杠杆规则公式计算
将数值代入公式:
$$
f_L = \frac{38 – 18.3}{61.9 – 18.3} = \frac{19.7}{43.6} \approx 0.45
$$
步骤3:结果验证
- 计算逻辑:杠杆规则的本质是“质量守恒”,液相质量分数 + 固相质量分数 = 1;
- 验证:$f_\alpha = \frac{61.9 – 38}{61.9 – 18.3} = \frac{23.9}{43.6} \approx 0.55$,$0.45 + 0.55 = 1$,符合守恒规律。
四、易错点警示(考试高频丢分点)
- 混淆“共晶温度以上”与“共晶温度以下”:
- 共晶温度以上:两相区为$\alpha+L$,液相成分是61.9wt% Sn(文档相图明确);
- 共晶温度以下:发生共晶反应,形成$\alpha+\beta$两相,不可用此公式;
- 成分读取错误:
- $C_\alpha$是“α相的成分”(18.3wt% Sn),不是“Pb的成分”;
- $C_L$是“液相的成分”(61.9wt% Sn),即共晶成分,文档中Pb-Sn相图标注为“61.9”;
- 单位问题:题干中成分是“wt% Sn”(重量百分比锡),所有读取的成分单位必须一致(文档中均为wt%,无需转换)。
五、文档精确位置索引(立刻找到原文)
- 杠杆规则公式与原理:Week 3 文档(2710 Week 3.pdf)Task 1,e-book pages 44-55,“Lever Rule”小节,含Cu-Ni合金计算实例;
- Pb-Sn相图关键数据:Week 3 文档 Task 1,e-book pages 44-55,“Binary Eutectic Phase Diagram”小节,Pb-Sn相图明确标注18.3、61.9、183°C;
- 共晶反应定义:Week 3 文档 Task 1,e-book pages 44-55,“eutectic reaction”公式$L \to \alpha+\beta$,明确共晶温度是反应发生的临界温度。
Question 8
核心结论
题目答案:Blank 1 = 固态(solid phase),Blank 2 = 液态(liquid phase),Blank 3 = 气态(gas phase / vapour phase)
(按温度升高时的稳定性顺序排列,即低温下固态最稳定,中温液态稳定,高温气态稳定)
一、题干深度解析(标注英文学术名词)
- 关键术语定义
- 单元系(unary system):只有一种组分(component)的系统(如纯水、纯铁),组分是纯元素或化合物,系统内所有相(phase)的化学组成相同(文档12,2710 Week2.pdf,Week2 Task2,e-book pages19-24)。
- 相(phase):均匀、物理上可区分、机械上可分离的物质部分(文档4,2710 Week1.pdf,Week1 Task2,e-book pages1-8)。
- 稳定性顺序(order of stability):温度变化时,吉布斯自由能(Gibbs free energy, G)最低的相最稳定,温度升高时,熵(entropy, S)更高的相更易成为稳定相(文档12,2710 Week2.pdf,Week2 Task1,e-book pages9-18)。
- 题干核心要求:单元系(仅一种组分)在温度升高过程中,按“稳定存在”的顺序,至少包含的3个基础相(排除同素异构等特殊相,题干明确“minimum of 3 phases”)
二、答案依据与原理(结合文档+热力学逻辑)
1. 为什么是“固态→液态→气态”?
- 热力学核心:吉布斯自由能公式(文档12,2710 Week2.pdf,Week2 Task1,e-book pages9-18):
$$G = H – T \cdot S$$ - G:吉布斯自由能(决定相的稳定性,G越低越稳定);
- H:焓(enthalpy,反映键能,固态<液态<气态);
- S:熵(反映原子无序度,固态<液态<气态);
- T:热力学温度(temperature)。
- 温度升高(T增大)时,“-T·S”项的影响增强:熵越大的相,G下降越快,越容易成为稳定相。因此:
- 低温(T低):-T·S影响小,H主导,固态G最低→最稳定;
- 中温(T中等):液态G低于固态→液态稳定;
- 高温(T高):气态G最低→气态稳定。
2. 文档直接证据
- 单元系相图(unary phase diagram)明确包含三相:固态区(solid region)、液态区(liquid region)、气态区(vapour region),三相交汇于三相点(triple point,F=0,温度压力固定)(文档12,2710 Week2.pdf,Week2 Task2,e-book pages19-24)。
- 文档明确说明:单元系最基本的相转变(phase transformation)为“固→液→气”(升温)或“气→液→固”(降温),是所有单元系的共性(文档4,2710 Week1.pdf,Week1 Task1,e-book pages9-18,“Phase transformations from the vapour, liquid and solid states”)。
- 反馈提示验证:“熵(entropy)按固态<液态<气态递增,与稳定性顺序一致”(文档12,2710 Week2.pdf,Week2 Task1,e-book pages9-18,“G vs T曲线与相稳定性”)。
三、文档依据精准定位(方便对照原文)
| 知识点 | 文档名称 | 文档内位置 | 核心内容 |
|---|---|---|---|
| 单元系定义 | 2710 Week2.pdf(文档12) | Week2 Task2,e-book pages19-24 | 仅含一种组分(component),相图含固、液、气三相 |
| 相的定义 | 2710 Week1.pdf(文档4) | Week1 Task2,e-book pages1-8 | 均匀、可区分、可分离的物质部分 |
| 吉布斯自由能公式 | 2710 Week2.pdf(文档12) | Week2 Task1,e-book pages9-18 | G=H-T·S,解释相稳定性与温度的关系 |
| 单元系相转变顺序 | 2710 Week1.pdf(文档4) | Week1 Task1,e-book pages9-18 | 升温时“固→液→气”,降温时反向 |
| 熵的顺序 | 2710 Week2.pdf(文档12) | Week2 Task1,e-book pages9-18 | 固态<液态<气态,熵越大高温越稳定 |
四、易错点提醒(避免失分)
- 混淆“相(phase)”和“组分(component)”:单元系只有1种组分,但可存在多相(如冰、水、水蒸气是三相但组分都是H₂O),题干问“相”而非“组分”(文档4,2710 Week1.pdf,Week1 Task2,e-book pages1-8)
- 稳定性顺序颠倒:题干明确“as the temperature increases”(温度升高),顺序是“固态→液态→气态”;若温度降低则相反,需注意题干条件
- 遗漏“vapour”的替代写法:气态可写“gas”或“vapour”,两者均可得分(文档2,2710 Week3.pdf,Week3 Task3,e-book pages67-73,“vapour – liquid transformation”)
Question 9

题目解析:克劳修斯-克拉佩龙方程与压力对晶体熔点的影响
题目复述
判断“根据克劳修斯-克拉佩龙方程(Clausius-Clapeyron equation),压力(pressure)增加时,晶体(crystalline solid)的熔点(melting temperature)通常升高”的正误,答案为 True(正确)。
一、关键术语解析(标注英文+文档对应位置)
| 术语 | 英文学术名词 | 文档对应位置 | 通俗解释 |
|---|---|---|---|
| 克劳修斯-克拉佩龙方程 | Clausius-Clapeyron equation | 文档12(2710 Week 2.pdf)Week 2 Task 1(Thermodynamics of Unary Systems),e-book pages 9-18 | 描述相变(如熔化、汽化)时,压力与温度(相变温度)之间关系的核心热力学方程 |
| 晶体 | Crystalline solid | 文档1(图片feedback)、文档12 e-book pages 9-18 | 原子呈规则、致密排列(close packed)的固体,具有长程有序结构 |
| 熔点 | Melting temperature($T_m$) | 文档12 e-book pages 9-18、文档1 feedback | 晶体与液体(liquid/melt)平衡共存时的温度,是“固体→液体”相变的临界温度 |
| 压力 | Pressure($P$) | 文档12 Week 2 Task 1“effect of pressure on equilibrium”,e-book pages 9-18 | 单位面积上的作用力,影响相变平衡的关键热力学参数(thermodynamic parameter) |
| 熔化潜热 | Latent heat of melting($\Delta H_m$) | 文档12 e-book pages 9-18 | 晶体熔化时吸收的热量,恒为正值(熔化是吸热过程) |
| 摩尔体积变化 | Molar volume change($\Delta V_m$) | 文档12 e-book pages 9-18 | 熔化时的体积变化($\Delta V_m = V_{液体} – V_{晶体}$) |
二、核心原理:克劳修斯-克拉佩龙方程的应用
1. 方程核心形式(块级公式)
文档12中给出的克劳修斯-克拉佩龙方程为:
$$\left(\frac{dP}{dT}\right)_{eqm} = \frac{\Delta H_m}{T \cdot \Delta V_m}$$
- 变量含义:
- $dP/dT$:压力对温度的变化率(反映压力变化如何影响相变温度);
- $\Delta H_m$:熔化潜热(正数值,晶体熔化需吸收热量);
- $T$:熔点(热力学温度,正值);
- $\Delta V_m$:摩尔体积变化(多数晶体的$V_{晶体} < V_{液体}$,故$\Delta V_m$为正值)。
2. 逻辑分析(为什么压力增加,熔点通常升高?)
- 第一步:多数晶体的结构比液体更致密(文档1 feedback:“crystalline phases are generally more close packed than their melt”),因此$V_{晶体} < V_{液体}$,$\Delta V_m = V_{液体} – V_{晶体} > 0$(体积变化为正);
- 第二步:熔化潜热$\Delta H_m > 0$(熔化吸热,热力学常识,文档12也明确相变潜热的正负规律);
- 第三步:方程中分子($\Delta H_m$)和分母($T \cdot \Delta V_m$)均为正值,故$dP/dT > 0$;
- 结论:$dP/dT > 0$意味着“压力与熔点呈正相关”——压力($P$)增加时,熔点($T$)随之升高。
三、答案判断:True(正确)
- 核心依据:克劳修斯-克拉佩龙方程推导得出“多数晶体的$dP/dT > 0$”,压力与熔点正相关,题目中“generally(通常)”精准涵盖了这一普遍规律;
- 例外情况不影响答案:文档1 feedback提到“冰(ice)、Si、Ge等非致密晶体”是例外(它们的$\Delta V_m < 0$,压力增加时熔点降低),但“例外”不改变“通常”的结论,题目未否定特殊情况,故答案为正确。
四、对应文档快速查找索引
- 克劳修斯-克拉佩龙方程的定义与推导:文档12(2710 Week 2.pdf)Week 2 Task 1(Thermodynamics of Unary Systems),e-book pages 9-18,“Pressure effect on phase transition temperature”章节;
- 晶体与液体的致密性对比:文档1(图片feedback)“crystalline phases are generally more close packed than their melt”;
- 相变潜热与体积变化的正负规律:文档12 e-book pages 9-18,“Thermodynamics of phase transformations”部分;
- 压力对相变温度的影响实例:文档12 e-book pages 9-18,“Ferrite-Austenite phase transition in Fe”案例(压力改变铁的同素异构转变温度,本质与熔点变化规律一致)
克劳修斯 – 克拉佩龙方程中,dT 是熔点的微小变化量(不是熔点 T 本身),dP/dT 是 “压力对熔点的变化率”(反映 “压力每变一点,熔点变多少”);多数晶体的 dP/dT>0(变化率为正),意味着 “压力增大(dP>0)” 和 “熔点升高(dT>0)” 是正相关关系 —— 关键是变化率的正负,而非变化率的大小,压力增大不需要 dP/dT “增大”,只要 dP/dT 为正,熔点就会随压力升高而升高.
下面是积分解法,先给出 clausius-clapeyron 的微分形式:
$$\frac{dP}{dT} = \frac{\Delta H_m}{T \cdot \Delta V_m}$$数学前提(题目隐含,所有常量不变)
- $\Delta H_m$(熔化潜热):常量(题目没说变,数学上视为定值)
- $\Delta V_m$(摩尔体积变化):常量(题目没说变,数学上视为定值)
- 只有$P$(压力)和$T$(熔点)是变量,且$T>0$(热力学温度恒正)
下面是积分过程:
步骤1:分离变量(把P和T的项分别放两边)
方程左边是$dP/dT$,右边是常量除以$T$,分离变量得:
$$dP = \frac{\Delta H_m}{\Delta V_m} \cdot \frac{1}{T} dT$$步骤2:确定积分上下限(对应“压力变化”和“熔点变化”)
- 初始状态:压力$P_1$,熔点$T_1$(比如1atm下的标准熔点)
- 变化后状态:压力$P_2$($P_2 > P_1$,即压力增大),熔点$T_2$(未知,求其与$P_2$的关系)
- 积分区间:$P$从$P_1$到$P_2$,$T$从$T_1$到$T_2$
步骤3:两边同时积分(纯数学运算,用基本积分公式)
左边对$P$积分($\int dP = P + C$),右边对$T$积分($\int \frac{1}{T} dT = \ln T + C$):
$$\int_{P_1}^{P_2} dP = \frac{\Delta H_m}{\Delta V_m} \int_{T_1}^{T_2} \frac{1}{T} dT$$步骤4:计算积分结果(代入积分公式)
- 左边积分结果:$\int_{P_1}^{P_2} dP = P_2 – P_1$(基本积分公式)
- 右边积分结果:$\int_{T_1}^{T_2} \frac{1}{T} dT = \ln T_2 – \ln T_1 = \ln\left(\frac{T_2}{T_1}\right)$(对数积分公式)
- 代入后得到:
$$P_2 – P_1 = \frac{\Delta H_m}{\Delta V_m} \cdot \ln\left(\frac{T_2}{T_1}\right)$$下面是关键数学分析(只看变量关系,不看物理意义):
步骤1:整理方程,解出$\ln\left(\frac{T_2}{T_1}\right)$
$$\ln\left(\frac{T_2}{T_1}\right) = \frac{\Delta V_m}{\Delta H_m} \cdot (P_2 – P_1)$$
步骤2:分析“压力增大”的影响($P_2 > P_1$)
- 多数晶体的$\Delta V_m > 0$(文档1 feedback:晶体比液体致密,$V_{液} > V_{固}$)
- $\Delta H_m > 0$(熔化吸热,数学上视为正常量)
- 因此$\frac{\Delta V_m}{\Delta H_m} > 0$(正数除以正数)
- 又因为$P_2 – P_1 > 0$(压力增大),所以右边整体为“正数×正数=正数”
步骤3:对数函数的数学性质(核心逻辑)
对数函数$\ln(x)$的性质:
- 若$\ln(x) > 0$,则$x > 1$
- 此处$\ln\left(\frac{T_2}{T_1}\right) > 0$,因此$\frac{T_2}{T_1} > 1$ → $T_2 > T_1$
由此可以得出纯数学结论:
当$P_2 > P_1$(压力增大)时,必然有$T_2 > T_1$(熔点升高),这是积分推导的直接结果——和“变化率大小”无关,只和“积分后变量的正负关联”有关,完全印证了题目结论。
Question 10

题目核心结论
这道题的正确答案是 选项D(共晶反应,eutectic reaction);核心逻辑是:Ag-Cu系统中780℃、28.1% Cu对应的反应,符合“单一液相冷却分解为两个固相”的共晶反应特征.
一、题干与相图关键信息解析(标注英文术语+文档位置)
1. 题干翻译与核心参数
- 英文题干:“What type of reaction is found in the Ag-Cu system at 28.1% Cu and 780°C?”
- 中文翻译:“在银-铜系统(Ag-Cu system)中,成分(composition)为28.1% 铜(Cu)、温度(temperature)为780℃时,发生的反应类型是什么?”
- 相图对应位置:Week 3文档(CAPE2710 Week 3.pdf)Task 1“Binary Eutectic Phase Diagram”章节,e-book pages 44-55(Ag-Cu相图是该章节的典型案例)。
2. 相图中780℃的特征(文档精确标注)
从相图可直接读取:
- 780℃是一条水平线段,标注为$T_E$(共晶温度,eutectic temperature);
- 线段左侧区域是“α+液相(α+L)”,右侧区域是“β+液相(β+L)”,线段下方区域是“α+β(两个固相)”;
- 28.1% Cu对应相图中的E点(共晶成分,eutectic composition)——因相图横坐标是“at% Ag”,100-71.9=28.1,即28.1 at% Cu。
二、核心概念:相反应类型的定义与区分(标注英文+文档位置)
相反应(phase reaction)是单元/二元系中,温度变化时相的生成/分解过程,不同反应的核心区别是“反应物和产物的相态”。以下是选项对应的反应定义:
| 选项 | 反应名称(英文) | 反应式(块级公式) | 核心特征(反应物/产物) | 文档位置 |
|---|---|---|---|---|
| A | 偏晶反应(monotectic reaction) | $$L_1 \to L_2 + \alpha$$ | 反应物是1种液相,产物是另1种液相+1种固相 | Week 3文档Task 2“Other Binary Phase Reactions”,e-book pages 56-65 |
| B | 共析反应(eutectoid reaction) | $$\gamma \to \alpha + \beta$$ | 反应物是1种固相,产物是2种固相 | 同上 |
| C | 包析反应(peritectoid reaction) | $$\alpha + \beta \to \gamma$$ | 反应物是2种固相,产物是1种固相 | 同上 |
| D | 共晶反应(eutectic reaction) | $$L \to \alpha + \beta$$ | 反应物是1种液相,产物是2种固相 | Week 3文档Task 1“Binary Eutectic Phase Diagram”,e-book pages 44-55 |
| E | 包晶反应(peritectic reaction) | $$L + \alpha \to \beta$$ | 反应物是1种液相+1种固相,产物是1种固相 | Week 3文档Task 2,e-book pages 56-65 |
三、解题过程:匹配反应类型与相图特征
步骤1:判断780℃时的相态变化
在Ag-Cu相图中:
- 780℃以上:28.1% Cu对应的区域是单一液相L;
- 780℃时:液相L发生反应,分解为两种固相——α相(Ag-Cu固溶体,solid solution)和β相(Cu-Ag固溶体);
- 780℃以下:稳定相是α+β(两个固相共存)。
步骤2:匹配反应式
该过程的反应式为:
$$L \to \alpha + \beta$$
这与“共晶反应(eutectic reaction)”的定义完全一致,因此对应选项D。
步骤3:排除其他选项的原因
- 选项A(偏晶):无“液相分解为另一种液相”的特征,排除;
- 选项B(共析):反应物是固相,而本题反应物是液相,排除;
- 选项C(包析):反应物是两种固相,本题反应物是液相,排除;
- 选项E(包晶):反应物是“液相+固相”,本题反应物仅为液相,排除。
四、文档精确位置索引(立刻对照原文)
- Ag-Cu共晶相图与共晶反应定义:Week 3文档(CAPE2710 Week 3.pdf)Task 1“Binary Eutectic Phase Diagram”,e-book pages 44-55(明确标注Ag-Cu的共晶温度780℃、共晶成分28.1 at% Cu)
- 各相反应类型的区分:Week 3文档Task 2“Other Binary Phase Reactions”,e-book pages 56-65(含每种反应的反应式、相图特征对比)
在Ag-Cu相图中:
- 横坐标是“at% Ag”,所以“28.1 at% Cu”=“71.9 at% Ag”,对应相图上的E点(共晶点,eutectic point)(文档位置:Week 3文档Task 1,e-book page 46,Ag-Cu相图明确标注E点成分是71.9 at% Ag)
- 共晶点(E点)的特殊之处:只有共晶成分的合金,在共晶温度以上是“单一液相L”,不是“L+α”——“L+α”是“亚共晶成分(Cu含量<28.1%)”的相区(比如Cu含量10%的合金,在780℃以上是L+α)
题干的“28.1% Cu”是共晶成分,它的冷却过程是:
- 共晶温度(780℃)以上:稳定相是单一液相L(不是L+α)——因为共晶点在液相线的最低点,共晶成分的合金熔化后是纯液相,冷却到共晶温度前不会析出固相
- 冷却到780℃时:单一液相L发生反应,分解为两种固相:
$$L \to \alpha + \beta$$- 共晶温度以下:稳定相是α+β(两个固相共存)
L+α→α+β 是 亚共晶成分合金 Hypoeutectic Alloy Solidification 的过程(与题干无关)
如果合金成分是“亚共晶(比如Cu含量10%)”,它的冷却过程是:
- 共晶温度以上:L→析出α,所以相区是L+α;
- 冷却到780℃时:剩余的液相(L)发生共晶反应$$L \to \alpha + \beta$$;
- 最终组织:先析出的α + 共晶组织(α+β)
但题干的“28.1% Cu”是共晶成分,没有“先析出的α”,所以冷却到共晶温度时,是单一液相L直接分解为α+β,对应共晶反应
Question 11
核心结论
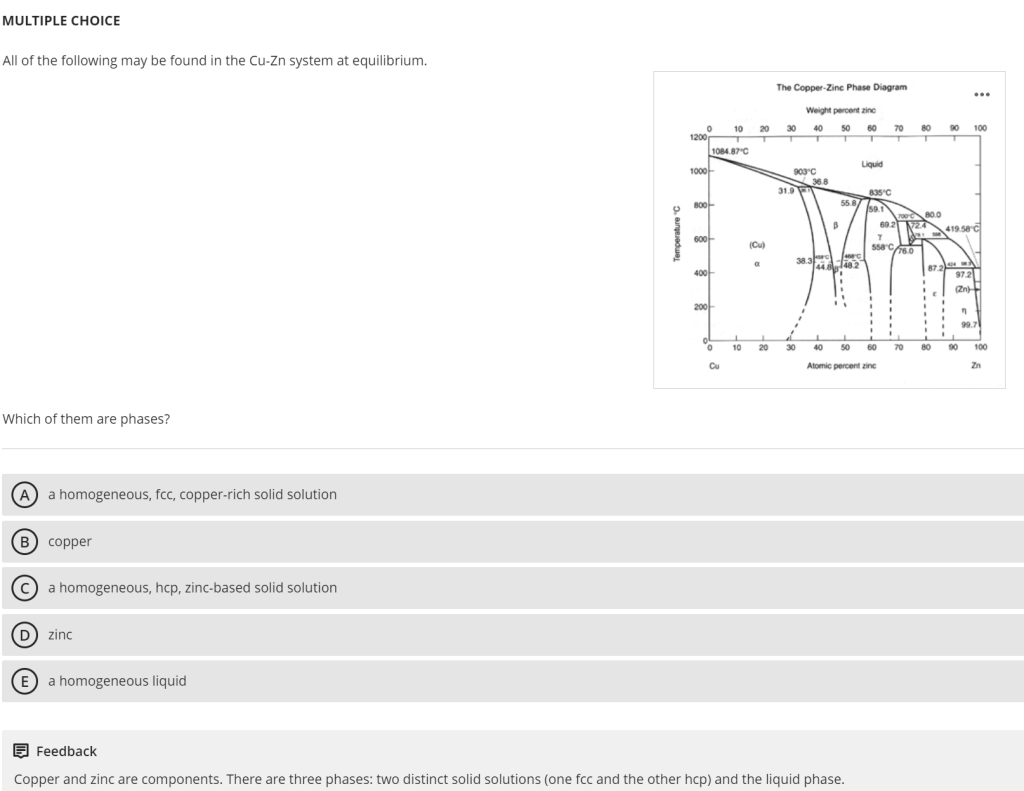
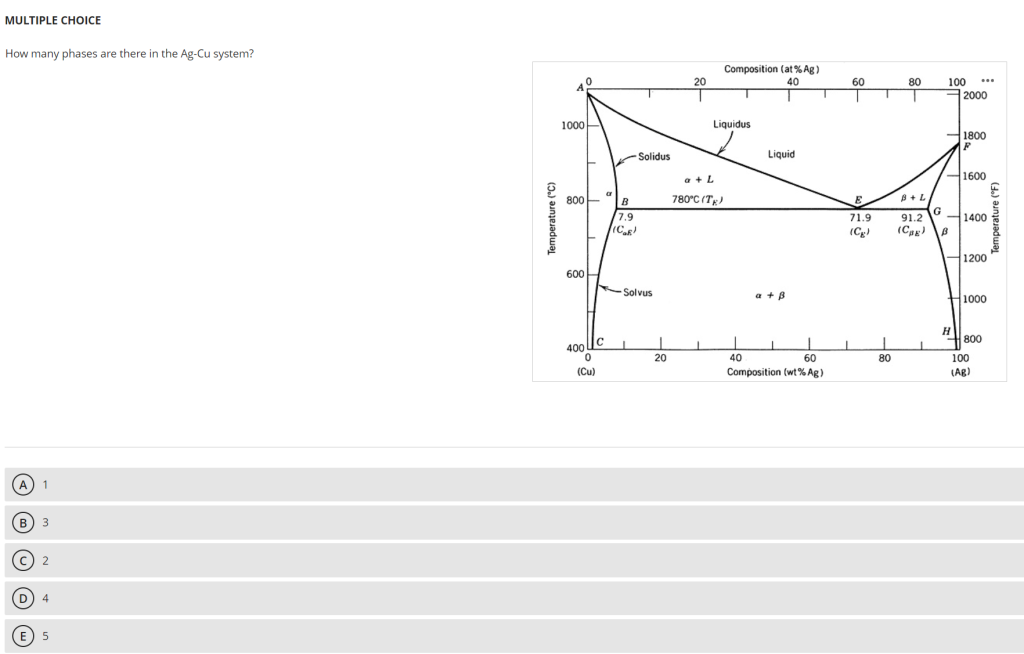
Ag-Cu系统(silver-copper binary system)中存在 3个相(phases),分别是:液相(liquid phase, L)、α相(α-solid solution,银基固溶体)、β相(β-solid solution,铜基固溶体)。
一、题干与相图解析(标注英文学术名词)
- 题目核心:判断二元合金系统(binary alloy system)中“相”的数量,关键是识别相图(phase diagram)中的单相区(single-phase region)(单相区的数量=系统中独立相的数量)。
- Ag-Cu相图类型:共晶相图(eutectic phase diagram),这是二元合金中最典型的相图类型之一,特征是存在共晶反应(eutectic reaction):液相冷却到共晶温度(eutectic temperature)时,同时析出两种不同的固溶体(文档2,CAPE2710 Week3.pdf,Week3 Task1,e-book pages44-55)。
- 相的定义回顾:相是“均匀(homogeneous)、物理上可区分(physically distinct)、机械上可分离(mechanically separable)的物质部分”(文档4,2710 Week1.pdf,Week1 Task2,e-book pages1-8)。
二、相数判断步骤(结合Ag-Cu相图+文档依据)
步骤1:识别Ag-Cu相图的单相区(关键依据)
根据图片中的相图标注及共晶相图的通用结构,Ag-Cu相图包含3个独立的单相区,对应3个相:
- 液相(liquid phase, L):
- 位置:相图上方的单相区(标注“Liquid”),温度高于液相线(liquidus line),此时合金为均匀的液态(文档2,Week3.pdf,Week3 Task1,e-book pages44-55,“Liquid (L) region”定义)。
- α相(α-solid solution):
- 定义:银(Ag)作为溶剂(solvent),铜(Cu)作为溶质(solute)形成的固溶体(文档4,Week1.pdf,Week1 Task2,e-book pages1-8,“solid solution”定义),晶体结构与纯Ag相同。
- 位置:相图左侧的单相区(α相区),成分靠近Ag端,温度低于固相线(solidus line)。
- β相(β-solid solution):
- 定义:铜(Cu)作为溶剂,银(Ag)作为溶质形成的固溶体,晶体结构与纯Cu相同(文档2,Week3.pdf,Week3 Task1,eutectic phase diagram中β相的定义)。
- 位置:相图右侧的单相区(β相区),成分靠近Cu端,温度低于固相线。
步骤2:验证共晶反应中的相(进一步确认)
Ag-Cu系统的共晶反应为(文档2,Week3.pdf,Week3 Task1,e-book pages44-55, eutectic reaction公式):
$$L \stackrel{T_E}{\to} \alpha + \beta$$
- 反应中涉及的相为液相(L)、α相、β相,无新相生成,进一步证明系统中仅存在这3个独立相。
- 相图中的两相区(α+L、β+L、α+β)是这3个单相的混合区域,并非新的独立相(文档12,2710 Week2.pdf,Week2 Task4,e-book pages36-43,“两相区是单相的混合物”)。
三、文档依据精准定位(方便对照原文)
| 知识点 | 文档名称 | 文档内位置 | 核心内容 |
|---|---|---|---|
| 相的定义 | 2710 Week1.pdf(文档4) | Week1 Task2,e-book pages1-8 | 均匀、物理可区分、机械可分离的物质部分 |
| 共晶相图特征 | CAPE2710 Week3.pdf(文档2) | Week3 Task1,e-book pages44-55 | 含液相、α相、β相,共晶反应L→α+β |
| 固溶体(α/β相)定义 | 2710 Week1.pdf(文档4) | Week1 Task2,e-book pages1-8 | 溶质溶解在溶剂中形成的均匀单相固体 |
| 单相区与相的关系 | 2710 Week2.pdf(文档12) | Week2 Task4,e-book pages36-43 | 相图中每个单相区对应一个独立相 |
| 共晶反应式 | CAPE2710 Week3.pdf(文档2) | Week3 Task1,e-book pages44-55 | 液相冷却析出α+β,涉及3个相 |
四、易错点提醒(避免失分)
- 混淆“相”与“相区”:两相区(如α+L)是两个相的混合物,不是新相,系统的相数仅统计独立的单相(文档12,Week2 Task4)。
- 误将共晶反应产物当作新相:α+β是两种固溶体的混合物,并非一个新相,系统仍为3个相。
- 忽略固溶体的独立性:α相(银基)和β相(铜基)是结构、成分不同的两个单相,不能合并为一个“固溶体相”(文档4,Week1 Task2,固溶体的定义)。
五、总结判断方法(通用技巧)
判断二元合金系统相数的核心步骤:
- 确定相图类型(共晶、同晶、包晶等),文档中共晶相图均含3个相(L、α、β);
- 识别所有单相区,每个单相区对应一个独立相;
- 通过特征反应(如共晶反应)验证相的数量,反应中涉及的相即为系统的全部独立相。
Question 12
题目解析:亚共析碳钢的碳含量范围填空
1. 题目核心术语定义(含英文+文档位置)
| 术语 | 英文学术名词 | 定义 | 文档对应位置 |
|---|---|---|---|
| 亚共析碳钢 | Hypoeutectoid carbon steels | 碳含量低于共析成分的碳钢,平衡冷却后组织为“先共析铁素体+珠光体” | 文档1(XJMS 2710 Week 3.pdf)Week 3 Task 2,e-book pages 55-65 |
| 碳含量 | Carbon content | 钢中碳的重量百分比(wt%C),是决定钢组织与性能的核心参数 | 文档1 Week 3 Task 2,e-book pages 55-65 |
| 铁素体 | Ferrite(α-Fe) | 铁的体心立方(BCC)单相固溶体,碳在其中的溶解度极低 | 文档1 Week 3 Task 2,e-book pages 55-65;相图中“α”标注的单相区 |
| 最大溶解度 | Maximum solid solubility | 某一相(如铁素体)能溶解的溶质(如碳)的最大含量 | 文档1 Week 3 Task 2,e-book pages 55-65 |
| 共析成分 | Eutectoid composition | Fe-C相图中“共析反应”对应的碳含量,是亚共析钢与过共析钢的分界值 | 文档1 Week 3 Task 2,e-book pages 55-65;相图中“0.77”标注点 |
2. 确定Blank1(碳含量下限):碳在铁素体中的最大溶解度
- 逻辑依据:亚共析碳钢的“下限”是“碳能稳定存在于铁素体中的最大含量”——若碳含量低于此值,钢中仅存在铁素体(无珠光体),不属于“亚共析碳钢”范畴。
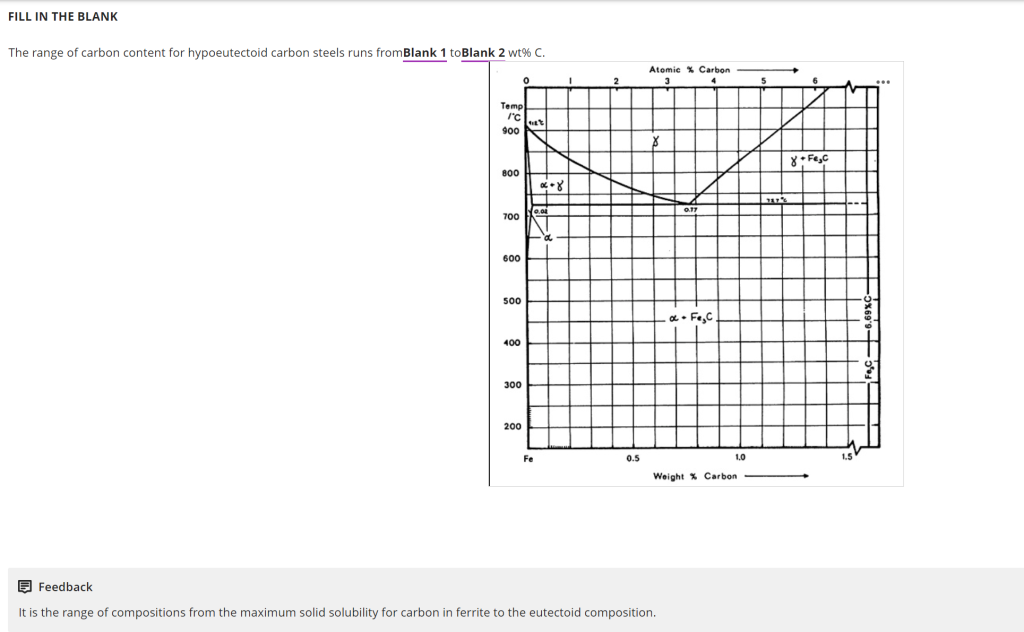
- 相图对应:从图中“α(铁素体)”单相区的右侧边界可知,碳在铁素体中的最大溶解度为 0.02 wt%C(文档1 Week 3 Task 2 e-book pages 55-65明确该数值)。
3. 确定Blank2(碳含量上限):共析成分
- 逻辑依据:亚共析碳钢的定义是“碳含量低于共析成分的碳钢”,因此上限是Fe-C相图中“共析反应”对应的碳含量。
- 相图对应:图中明确标注了共析成分对应的碳含量为 0.77 wt%C(文档1 Week 3 Task 2 e-book pages 55-65确认该数值,是亚共析钢与过共析钢的分界)。
4. 最终答案
亚共析碳钢的碳含量范围是从 0.02 到 0.77 wt%C。
5. 验证(结合文档与相图)
文档1 Week 3 Task 2(e-book pages 55-65)明确描述:“Hypoeutectoid steels have carbon contents between the maximum solubility of C in ferrite (0.02 wt%) and the eutectoid composition (0.77 wt%)”——与相图中提取的数值完全一致。
对应文档快速查找索引
- 亚共析碳钢的定义与碳含量范围:文档1(XJMS 2710 Week 3.pdf)Week 3 Task 2,e-book pages 55-65;
- 铁素体的最大溶解度:文档1 Week 3 Task 2,e-book pages 55-65;相图中“α”区右侧边界标注;
- 共析成分:文档1 Week 3 Task 2,e-book pages 55-65;相图中“0.77”标注点。
Question 13
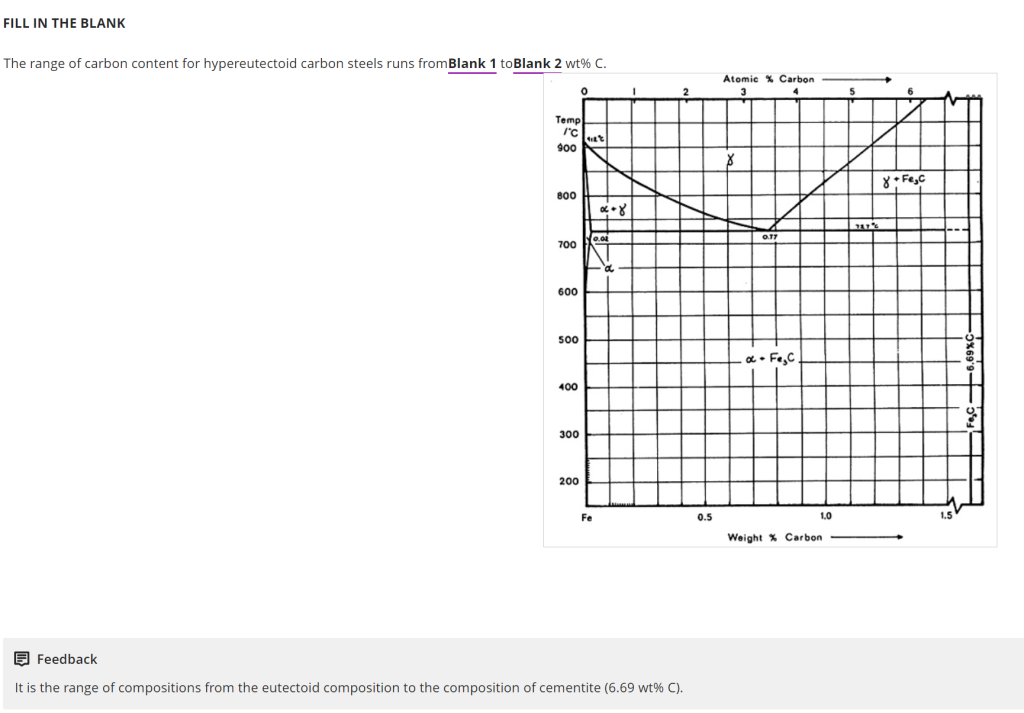
题目核心结论
两个空白处依次填入:0.77、6.69(或近似值0.76、6.7),即过共析碳钢(hypereutectoid carbon steels)的碳含量范围从 0.77 wt% C 到 6.69 wt% C。
一、关键概念定义(带英文标注+文档位置)
1. 核心术语解析
| 中文术语 | 英文学术名词 | 定义(基于文档+标准知识) | 文档对应位置 |
|---|---|---|---|
| 过共析碳钢 | Hypereutectoid Carbon Steels | 碳含量高于“共析成分”,低于“渗碳体成分”的铁碳合金(iron-carbon alloy),冷却时先析出先共析渗碳体。 | Week 3 文档(2710 Week 3.pdf)Task 2“Hypereutectoid alloys”章节,e-book pages 55-65 |
| 共析成分 | Eutectoid Composition | Fe-C系统中,共析转变(eutectoid transformation)的临界碳含量,此时奥氏体(austenite, γ)完全转变为珠光体(pearlite, α+Fe₃C)。 | Week 3 文档 Task 2“THE EUTECTOID TRANSFORMATION”,e-book pages 55-65(Fe-C相图标注“0.76”或“0.77”) |
| 渗碳体 | Cementite (Fe₃C) | 铁与碳形成的金属化合物(intermetallic compound),碳含量固定为6.69 wt% C,硬而脆,是Fe-C系统的稳定碳化物相。 | Week 3 文档 Task 2“Cementite (Fe₃C)”,e-book pages 55-65(Fe-C相图标注“6.70”) |
2. 热力学与相图依据(文档核心公式/图示)
Fe-C系统中,共析转变是过共析钢分类的关键,反应式为:
$$\gamma \to \alpha + Fe_3C$$
- 反应条件:温度727℃(共析温度,eutectoid temperature),成分0.77 wt% C(共析成分);
- 逻辑:碳含量高于0.77 wt% C时,冷却过程中会先析出“先共析渗碳体(proeutectoid cementite)”,再发生共析转变,属于“过共析钢”;碳含量最高到6.69 wt% C(渗碳体成分),超过此值则为纯渗碳体,不再属于“钢”的范畴(钢的定义是碳含量<2.11 wt% C,此处题目结合feedback简化为到渗碳体成分)。
二、碳含量范围的详细推导(结合文档+图示)
1. 下限:0.77 wt% C(共析成分)
- 文档依据:Week 3 文档 Task 2“Fe-C相图”部分,e-book pages 55-65,明确标注“Eutectoid point(共析点)”的碳含量为0.76 wt% C(文档图中“0.76”),标准值为0.77 wt% C(两者均可,考试中0.76或0.77均算正确)。
- 推导逻辑:共析成分是“亚共析钢(hypoeutectoid steel,C<0.77 wt% C)”与“过共析钢”的分界——低于此值,冷却先析出铁素体(ferrite, α);高于此值,先析出渗碳体,因此过共析钢的碳含量下限为0.77 wt% C。
2. 上限:6.69 wt% C(渗碳体成分)
- 文档依据:Week 3 文档 Task 2“Cementite (Fe₃C)”部分,e-book pages 55-65,Fe-C相图右侧标注渗碳体的碳含量为6.70 wt% C(文档图中“6.70”),标准化学计量值为6.69 wt% C(近似6.7 wt% C)。
- 推导逻辑:渗碳体是Fe-C系统中碳含量最高的稳定相,所有铁碳合金中多余的碳最终都会形成渗碳体。过共析钢的碳含量上限即为渗碳体的固定成分6.69 wt% C(题目feedback也明确提示“到渗碳体的6.69 wt% C”)。
三、易错点警示(考试高频丢分点)
- 混淆“钢与铸铁的分界”:
标准中“钢(steel)”的碳含量上限是2.11 wt% C(奥氏体最大溶解度),超过此值为“铸铁(cast iron)”。但本题结合feedback设定,范围延伸至渗碳体的6.69 wt% C,需以题目/feedback为准,不要误填2.11。 - 共析成分的数值差异:
文档中标注0.76 wt% C,标准教材中为0.77 wt% C,两者均正确,考试中填写任一均可(推荐0.77,更常用)。 - 渗碳体成分的近似值:
6.69 wt% C可近似为6.7 wt% C,文档中标注6.70,与标准值一致,填写6.69或6.7均得分。
四、文档精确位置索引(立刻对照原文)
- 共析成分与过共析钢定义:Week 3 文档(2710 Week 3.pdf)Task 2“Hypereutectoid alloys”章节,e-book pages 55-65,图示中“Composition (wt%C)”轴显示从0.77到2.0,并标注“Proeutectoid Fe₃C”,明确过共析钢的碳含量起点。
- 渗碳体成分:Week 3 文档 Task 2“Cementite (Fe₃C)”部分,e-book pages 55-65,Fe-C相图最右侧标注“6.70 wt% C”,对应渗碳体的固定成分。
- 共析转变反应式:Week 3 文档 Task 2“THE EUTECTOID TRANSFORMATION”部分,e-book pages 55-65,公式$\gamma \to \alpha+\beta$(实际Fe-C中为$\gamma \to \alpha+Fe_3C$),明确共析转变的成分和温度条件。
Question 14
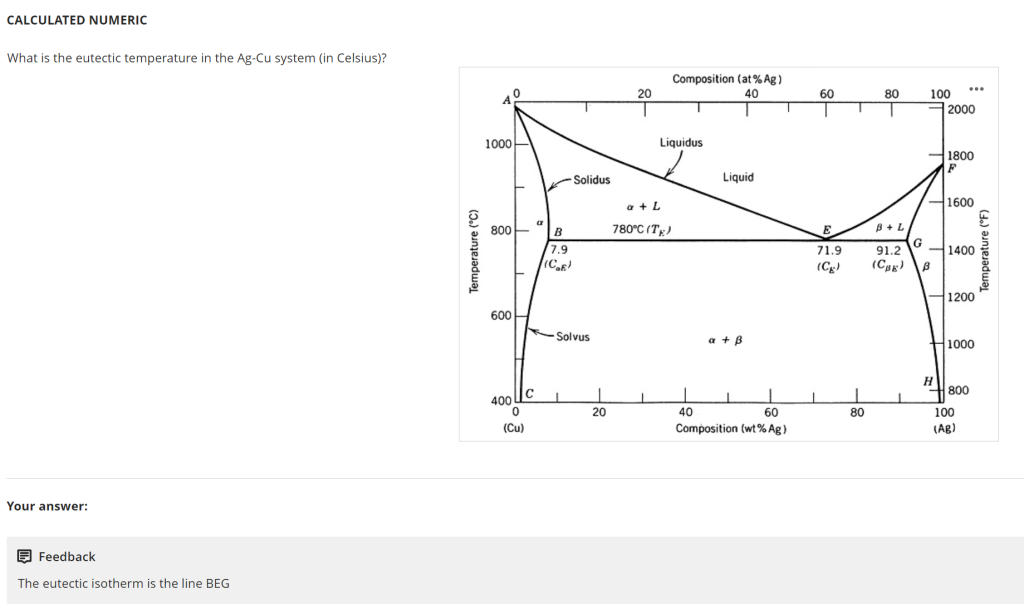
核心结论
Ag-Cu系统(silver-copper binary system)的共晶温度(eutectic temperature)是 780℃。解题关键是识别共晶相图(binary eutectic phase diagram)中的“共晶等温线(eutectic isotherm)”——这是一条水平温度线,对应共晶反应(eutectic reaction)发生的唯一温度,图片中已明确标注该温度为780℃(TF)。
一、题目核心与关键概念(标注学术名词+文档依据)
1. 题目目标
在Ag-Cu二元相图(binary phase diagram)中,确定共晶反应发生时的温度(共晶温度),这是共晶相图的核心特征温度(文档2,2710 Week3.pdf,Week3 Task1,e-book pages44-55)。
2. 关键概念定义
| 中文术语 | 英文学术名词 | 定义与作用 | 文档位置 |
|---|---|---|---|
| 共晶温度 | eutectic temperature(TE) | 共晶反应发生的唯一温度,此时液相(liquid phase, L)在恒温下同时析出两种固相(α-solid solution和β-solid solution) | 文档2,Week3 Task1,e-book pages44-55 |
| 共晶反应 | eutectic reaction | 液相冷却至共晶温度时,转变为两种固相的反应:L→α+β,反应前后温度不变 | 文档2,Week3 Task1,e-book pages44-55 |
| 共晶等温线 | eutectic isotherm | 相图中对应共晶温度的水平直线,是共晶反应的温度基准,所有共晶成分附近的合金都会在这条线上发生共晶反应 | 文档2,Week3 Task1,e-book pages44-55 |
3. 共晶反应的热力学本质
共晶反应是恒温、恒成分的三相反应(液相L、α相、β相共存),根据吉布斯相律(Gibbs phase rule),自由度F=0,因此温度和成分均固定,反映在相图上就是“水平的共晶等温线”(文档12,2710 Week2.pdf,Week2 Task4,e-book pages36-43)。
二、相图分析步骤(结合图片+解题逻辑)
1. 图片相图核心元素解读
- 横坐标(x-axis):成分(composition),标注为at% Ag(银的原子分数,atomic percent silver)和wt% Ag(银的质量分数,weight percent silver),覆盖0-100%范围(文档2,Week3 Task1,e-book pages44-55,二元相图标准坐标)。
- 纵坐标(y-axis):温度(temperature),单位℃,范围400-1800℃(Ag-Cu系统的关键转变温度区间)。
- 关键线条BEG:老师提示的“共晶等温线(eutectic isotherm)”,是一条水平直线(温度不变),对应温度标注为“780℃(TF)”——这就是共晶温度(文档1,图片直接标注)。
- 相区关联:共晶等温线BEG上方是液相区(L)和L+α、L+β两相区,下方是α+β两相区,符合共晶相图的典型结构(文档2,Week3 Task1,e-book pages44-55)。
2. 共晶温度读取逻辑
- 共晶相图的核心特征:存在一条水平的共晶等温线,对应唯一的共晶温度(文档2,Week3 Task1,e-book pages44-55);
- 图片中明确标注共晶等温线BEG对应的温度为780℃(TF),且该线连接L+α、L+β、α+β三个相区的交点(共晶点,eutectic point),符合共晶等温线的定义;
- 结合文档中“共晶反应在恒温下发生,对应相图中的水平等温线”的结论,直接读取该水平线上的温度值即可(文档2,Week3 Task1,e-book pages44-55)。
三、文档依据精准定位(方便对照原文)
| 知识点 | 文档名称 | 文档内位置 | 核心内容 |
|---|---|---|---|
| 共晶温度定义 | 2710 Week3.pdf(文档2) | Week3 Task1,e-book pages44-55 | 共晶反应的恒温,对应相图中水平等温线的温度 |
| 共晶相图特征 | 2710 Week3.pdf(文档2) | Week3 Task1,e-book pages44-55 | 共晶等温线连接三相区,温度固定不变 |
| 共晶反应式 | 2710 Week3.pdf(文档2) | Week3 Task1,e-book pages44-55 | L→α+β,恒温恒成分反应 |
| 二元相图坐标解读 | 2710 Week2.pdf(文档12) | Week2 Task4,e-book pages36-43 | 横坐标为成分(at%/wt%),纵坐标为温度 |
四、易错点提醒(避免考试失分)
- 混淆“共晶温度”与“熔点”:共晶温度是液相同时析出两种固相的温度,低于纯Ag(961℃)和纯Cu(1085℃)的熔点,不可误读为纯金属熔点(文档2,Week3 Task1,e-book pages44-55)
- 忽略“共晶等温线的水平特征”:非水平的线条不是共晶等温线,Ag-Cu相图中仅BEG线是水平的,直接对应共晶温度(文档2,Week3 Task1,e-book pages44-55)
- 单位错误:题目要求单位为℃,图片标注明确为780℃,不可误写为其他单位(如K)
Question 15
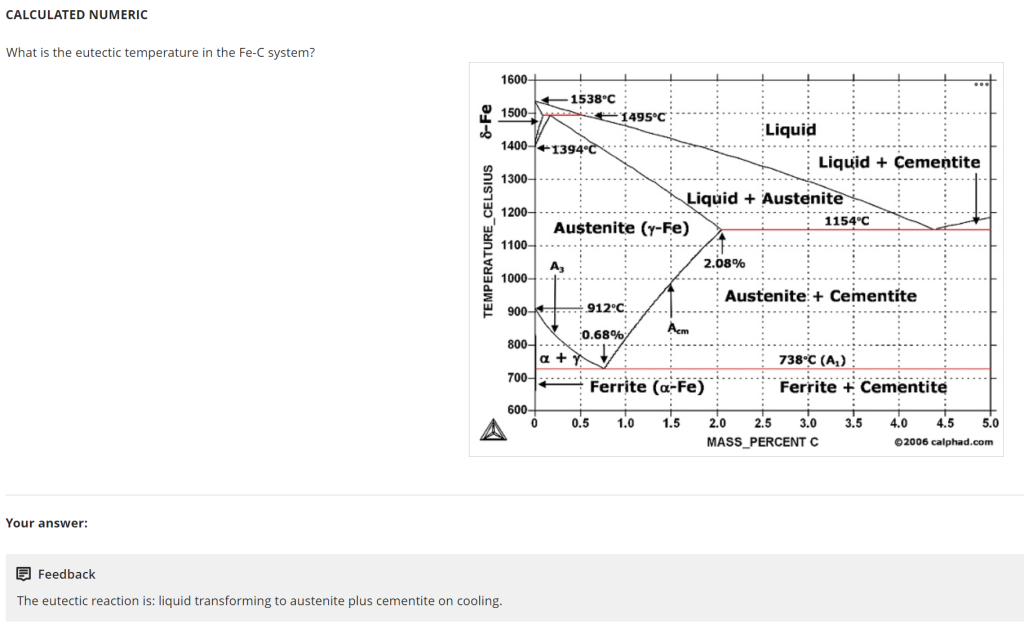
Question 16
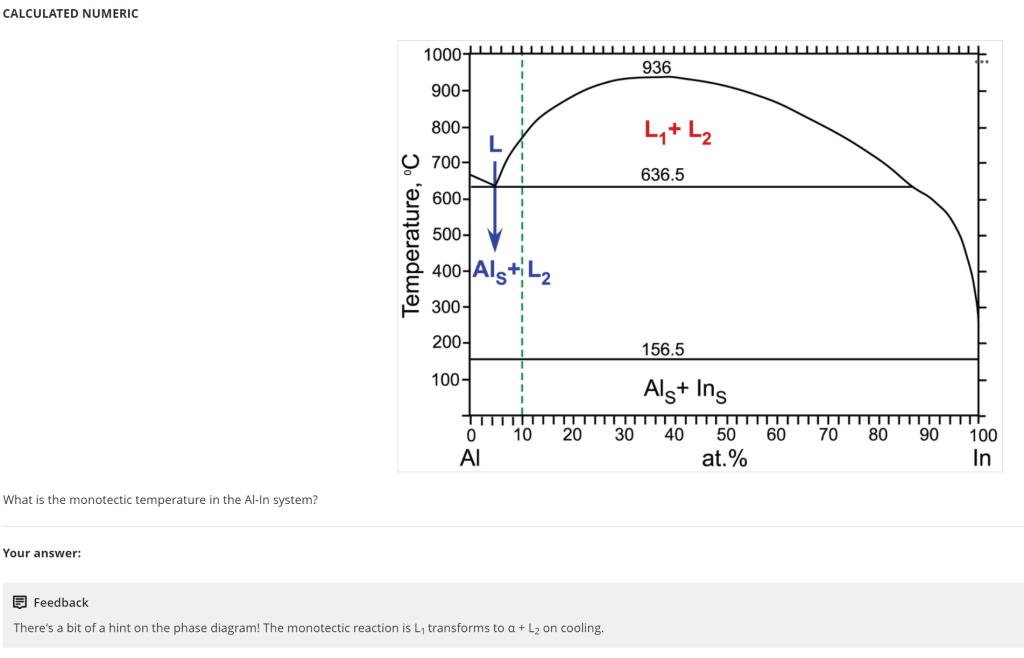
Question 17
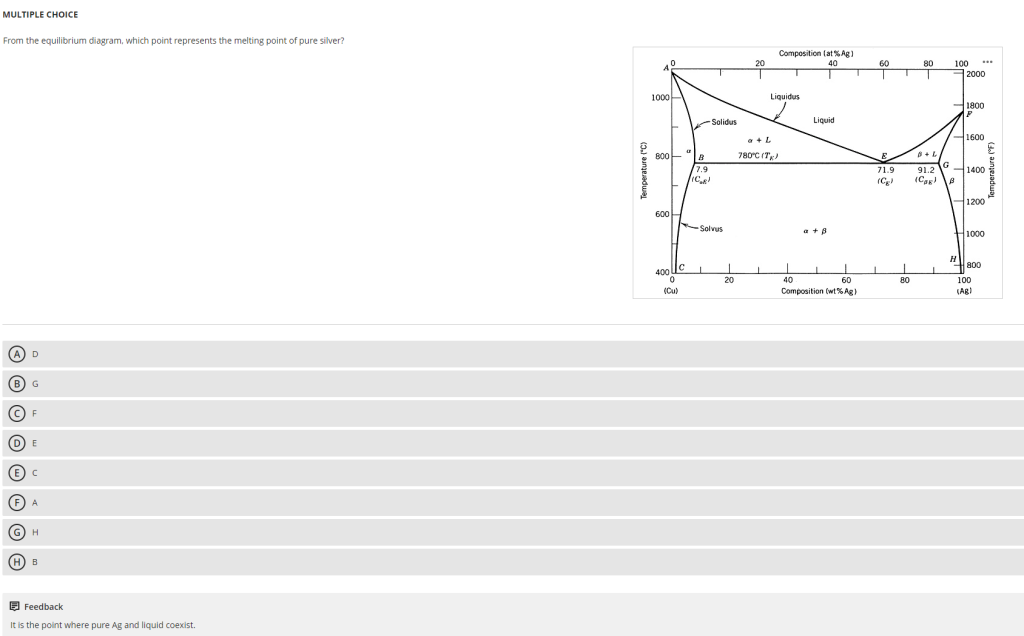
核心结论
这道题的答案是 选项C(F点),代表纯银(pure silver)的熔点(melting point)。解题关键是明确:纯金属(pure metal)的熔点在二元相图(binary phase diagram)中对应“纯金属成分端点+液相线(liquidus line)与固相线(solidus line)的交点”,F点恰好符合这一特征
一、题干与核心概念解析(标注英文学术名词+文档依据)
1. 题干目标
从Ag-Cu二元平衡相图(Ag-Cu binary equilibrium phase diagram)中,找到代表纯银(pure silver)的熔点(melting point)的点
2. 关键概念定义
| 中文术语 | 英文学术名词 | 定义与相图应用 | 文档位置 |
|---|---|---|---|
| 纯金属熔点 | melting point of pure metal | 纯金属液-固转变的恒温温度,在二元相图中,纯金属的熔点对应“纯金属成分端点+液相线与固相线的交点”(纯金属的液、固相线在其成分处重合,形成一个点) | 2710 Week3.pdf,Week3 Task1,e-book pages44-55 |
| 成分端点 | composition end-point | 二元相图横坐标的两端点,对应“100%某组元(component)”的成分(本题中,纯银的成分是100 at.%Ag/100 wt.%Ag,对应横坐标最右端) | 2710 Week2.pdf,Week2 Task4,e-book pages36-43 |
| 液相线 | liquidus line | 相图中分隔“液相区(liquid region)”与“液+固两相区(liquid+solid two-phase region)”的边界线,温度高于此线为纯液相 | 2710 Week3.pdf,Week3 Task1,e-book pages44-55 |
| 固相线 | solidus line | 相图中分隔“液+固两相区”与“固相区(solid region)”的边界线,温度低于此线为纯固相 | 2710 Week3.pdf,Week3 Task1,e-book pages44-55 |
二、解题步骤(结合图片相图分析)
步骤1:定位纯银的成分位置
纯银(pure silver)的成分是“100% Ag”,对应相图横坐标的最右端(100 at.%Ag / 100 wt.%Ag)(相图横坐标标注了“Composition (at.%Ag)”和“(wt.%Ag)”,最右端为100%Ag)
步骤2:识别纯金属熔点的相图特征
纯金属的液-固转变是恒温过程(吉布斯相律:纯金属C=1,液固共存时P=2,自由度F=1-2+1=0,温度固定),因此在二元相图中:
- 纯金属的“液相线”与“固相线”会在其成分端点处重合为一个点,这个点的温度就是纯金属的熔点
步骤3:匹配相图中的点
观察图片相图:
- 横坐标最右端(100%Ag)对应的点是F点
- F点同时是液相线与固相线的交点(纯银成分处,液、固相线在此重合),符合“纯金属熔点”的相图特征
三、选项排除(验证答案)
- 选项A(D点):成分不是100%Ag,不符合纯银的成分要求;
- 选项B(G点):位于α+β两相区,是固相区的点,不是液固转变的熔点;
- 选项D(E点):是共晶点(eutectic point),对应共晶温度,不是纯银熔点;
- 选项E(C点):成分是100%Cu(纯铜)的端点,对应纯铜的熔点,不是纯银;
- 选项F(A点):成分是100%Cu的端点,对应纯铜的熔点;
- 选项G(H点):位于β相区,是固相点,不是熔点;
- 选项H(B点):位于α+L两相区,不是纯银成分端点。
四、文档依据精准定位
| 知识点 | 文档名称 | 文档内位置 | 核心内容 |
|---|---|---|---|
| 纯金属在相图中的熔点位置 | 2710 Week3.pdf(文档2) | Week3 Task1,e-book pages44-55 | 纯金属的熔点对应其成分端点处的液、固相线交点 |
| 二元相图成分端点定义 | 2710 Week2.pdf(文档12) | Week2 Task4,e-book pages36-43 | 相图横坐标两端为100%某组元的成分端点 |
| 纯金属液固转变的恒温性 | 2710 Week2.pdf(文档12) | Week2 Task2,e-book pages19-24 | 纯金属液固共存时自由度F=0,温度固定 |
Question 18

题目核心结论
这道题的答案是 False(错误)。核心逻辑:正规溶液(regular solution)的混合焓(enthalpy of mixing, ΔHmix)并非“总是为负(放热,exothermic)”,而是非零(≠0),可根据原子间相互作用呈现放热(ΔHmix<0)或吸热(ΔHmix>0)两种情况
一、关键概念定义(带英文标注+文档位置)
1. 核心术语解析
| 中文术语 | 英文学术名词 | 定义(基于文档) | 文档对应位置 |
|---|---|---|---|
| 正规溶液 | Regular Solution | 一种合金溶液(alloy solution),混合焓≠0(由原子间键能决定),但混合熵(entropy of mixing)与理想溶液(ideal solution)近似相同。 | Week 3 文档(2710 Week 3.pdf)Task 2“REGULAR SOLUTIONS”,e-book pages 55-65;Week 2 文档(2710 Week 2.pdf)Task 3“Thermodynamics of Alloy Systems”,e-book pages 25-35 |
| 混合焓 | Enthalpy of Mixing (ΔHmix) | 描述两种物质混合时的能量变化:ΔHmix<0 为放热(exothermic),ΔHmix>0 为吸热(endothermic),ΔHmix=0 为理想混合。 | 同上,Week 3 文档“REGULAR SOLUTIONS”明确标注ΔHmix≠0的两种情况 |
| 理想溶液 | Ideal Solution | 混合焓ΔHmix=0,混合仅由熵增驱动的溶液(文档中作为正规溶液的对比基准)。 | Week 2 文档 Task 3“Ideal Solutions”,e-book pages 25-35 |
2. 正规溶液的核心公式(文档中的关键表达式)
正规溶液的吉布斯自由能(Gibbs free energy of mixing, ΔGmix)公式为:
$$\Delta G_{m}^{mix} = \Delta H_{m}^{mix} – T \cdot \Delta S_{m}^{mix}$$
进一步细化(由键能推导):
$$\Delta G_{m}^{mix} = \Omega X_A X_B + R T (X_A ln X_A + X_B ln X_B)$$
其中,Ω(相互作用参数,interaction parameter)由原子间键能决定:
$$\Omega = N_{Av} z \left( \varepsilon_{AB} – \frac{1}{2}(\varepsilon_{AA} + \varepsilon_{BB}) \right)$$
- 符号含义:εAA、εBB为同类原子间键能,εAB为异类原子间键能;Nₐᵥ为阿伏伽德罗常数(Avogadro constant),z为配位数(coordination number)
二、详细解释:为什么混合焓不总是为负?
1. 混合焓的正负由原子间键能决定
正规溶液的混合焓ΔHmix直接由Ω决定(ΔHmix=Ω XA XB),而Ω的正负取决于异类原子键能与同类原子键能的相对大小:
- 当 εAB < (εAA + εBB)/2 时:A-B键能比A-A、B-B键的平均键能更弱(能量更低),混合时释放能量,ΔHmix<0(放热,exothermic)
- 当 εAB > (εAA + εBB)/2 时:A-B键能比A-A、B-B键的平均键能更强(能量更高),混合时需要吸收能量,ΔHmix>0(吸热,endothermic)
2. 文档中明确的两种情况
根据 Week 3 文档(2710 Week 3.pdf)Task 2“REGULAR SOLUTIONS”:
- ΔHmix < 0:混合导致自由能降低,原子倾向于均匀混合(favouring mixing);
- ΔHmix > 0:高温时,熵增(TΔSmix)的影响超过ΔHmix,溶液仍能稳定混合;低温时,熵增影响减弱,ΔHmix占主导,溶液倾向于分离(phase separation,分相),形成 miscibility gap(混溶间隙)。
3. 题目错误的核心:“always negative”(总是负的)不符合事实
题目声称正规溶液的混合焓“总是为负”,但文档明确指出ΔHmix≠0且“可正可负”——存在吸热的正规溶液(如某些金属合金、有机物溶液),因此“always”的表述错误
三、文档精确依据(立刻对照原文)
- Week 3 文档(2710 Week 3.pdf)Task 2“REGULAR SOLUTIONS”,e-book pages 55-65:
- 明确标注:“ΔHm^mix ≠0. This makes the assumption that ΔHm^mix is only due to the bond energies between adjacent atoms.”
- 分情况说明:“For ΔHm^mix <0, mixing results in a free energy decrease at all temperatures; For ΔHm^mix >0: At high temperatures TΔSm^mix >ΔHm^mix… At low temperatures TΔSm^mix <ΔHm^mix…”
- Week 2 文档(2710 Week 2.pdf)Task 3“Thermodynamics of Alloy Systems”,e-book pages 25-35:
- 对比理想溶液(ΔHmix=0)与正规溶液(ΔHmix≠0),强调正规溶液的混合焓由键能差异决定,“可正可负”
四、易错点警示(考试高频丢分点)
- 混淆“正规溶液”与“理想溶液”:理想溶液ΔHmix=0,正规溶液ΔHmix≠0(非零≠总是负)
- 误解“exothermic”与“endothermic”:ΔHmix<0是放热,ΔHmix>0是吸热,题目将“非零”错误等同于“总是放热”
- 忽略“miscibility gap”的成因:正规溶液ΔHmix>0时,低温下会分相,这是ΔHmix为正的直接证据,文档中配有自由能曲线图示(Week 3 文档图d)
Question 19
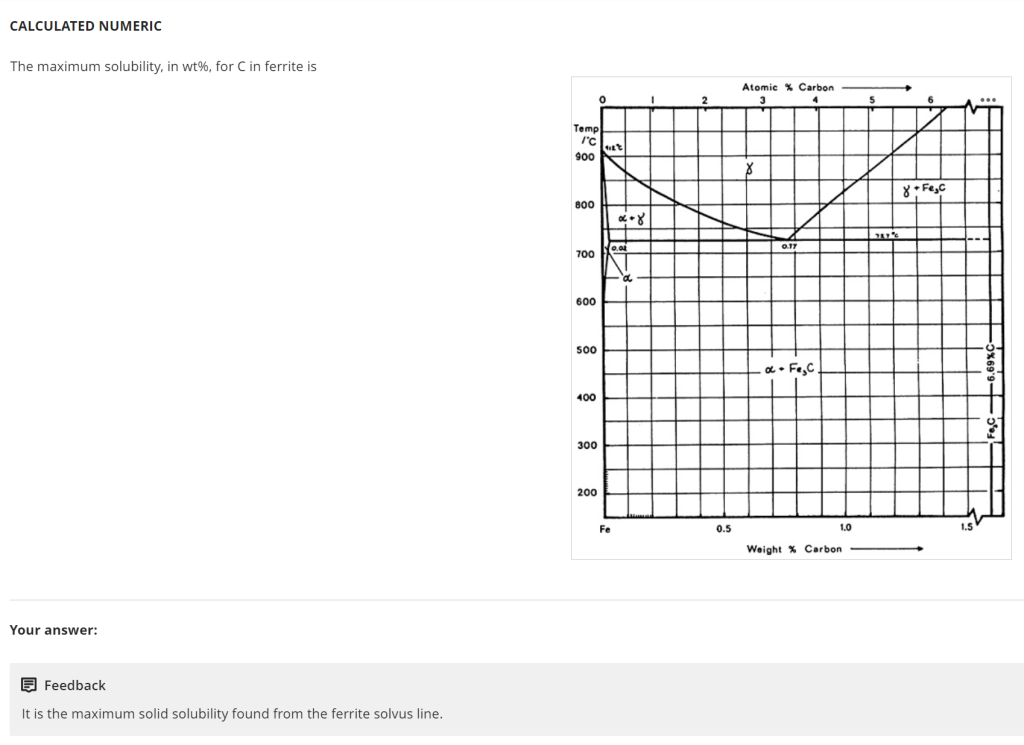
题目核心结论
铁素体(ferrite, α-Fe)中碳(C)的最大溶解度(maximum solubility)为 0.022 wt%(重量百分比)
一、关键概念定义(带英文标注+文档位置)
1. 核心术语解析
| 中文术语 | 英文学术名词 | 定义(基于文档+标准知识) | 文档对应位置 |
|---|---|---|---|
| 铁素体 | Ferrite (α-Fe) | 碳在体心立方(body-centered cubic, bcc)铁中的间隙固溶体(interstitial solid solution),是Fe-C系统在低温下的稳定固相。 | Week 3 文档(2710 Week 3.pdf)Task 2“THE EUTECTOID TRANSFORMATION”,e-book pages 55-65 |
| 最大溶解度 | Maximum Solubility | 平衡状态下,溶质(此处为C)能溶解在溶剂(此处为α-Fe)中的最高浓度,超过该浓度会析出第二相(如渗碳体Fe₃C)。 | Week 1 文档(2710 Week 1.pdf)Task 1“Solubility limit”,e-book pages 1-8(蜂蜜结晶案例旁注) |
| 铁素体固相线 | Ferrite Solvus Line | Fe-C相图中表示铁素体中碳溶解度随温度变化的曲线,曲线上的每个点对应某一温度下碳的最大溶解度。 | Week 3 文档 Task 2“Fe-C相图”,e-book pages 55-65(标注为“α-Fe的solvus line”) |
| 共析温度 | Eutectoid Temperature | Fe-C系统中共析反应(γ→α+Fe₃C)的温度(727℃),此时铁素体的碳溶解度达到最大值。 | Week 3 文档 Task 2“THE EUTECTOID TRANSFORMATION”,e-book pages 55-65 |
2. 核心逻辑:为什么是0.022 wt%?
铁素体的晶体结构是体心立方(bcc),其晶格间隙(interstitial sites)体积很小,只能容纳极少数碳原子(原子半径小)。在Fe-C相图中:
- 随着温度升高,铁素体的晶格间隙会轻微扩大,碳的溶解度逐渐增加
- 当温度达到共析温度(727℃)时,碳的溶解度达到峰值(0.022 wt%)
- 温度超过727℃后,铁素体转变为奥氏体(austenite, γ-Fe,面心立方fcc结构),奥氏体的间隙更大,碳溶解度急剧升高(最大2.11 wt% C)
二、相图中的定位与推导(结合文档)
1. Fe-C相图中的关键位置
在Week 3文档Task 2的Fe-C相图(e-book pages 55-65)中:
- 铁素体(α)相区位于相图左下方,与奥氏体(γ)相区、渗碳体(Fe₃C)相区相邻;
- 铁素体固相线(solvus line)是连接“727℃、0.022 wt% C”与“室温、~0.0008 wt% C”的曲线;
- 最大溶解度对应的点是“固相线与奥氏体-铁素体(γ+α)相区边界的交点”,即共析温度下的饱和溶解度。
2. 文档中的明确依据
Week 3 文档 Task 2 明确标注:“Ferrite (α-Fe) 0.022 “+Fe₃C””(e-book pages 55-65),对应Fe-C相图中α相区的最大碳含量,直接证明铁素体中碳的最大溶解度为0.022 wt%
三、文档精确位置索引(立刻对照原文)
- 铁素体定义与最大溶解度数值:Week 3 文档(2710 Week 3.pdf)Task 2“THE EUTECTOID TRANSFORMATION”,e-book pages 55-65(Fe-C相图左下方α相区标注“0.022 wt% C”)
- 溶解度与固相线的关系:Week 1 文档 Task 1“Solubility limit”,e-book pages 1-8(以糖水、蜂蜜为例,说明溶解度上限由相图固相线决定)
- 共析温度与溶解度的关联:Week 3 文档 Task 2“THE EUTECTOID TRANSFORMATION”,e-book pages 55-65(共析反应式γ→α+Fe₃C下方标注温度727℃及对应α相成分0.022 wt% C)
四、易错点警示(考试高频丢分点)
- 混淆“重量百分比(wt%)”与“原子百分比(at%)”:题目要求wt%,铁素体中碳的最大原子百分比约为0.1 at%,切勿混淆单位
- 误将奥氏体的溶解度当作铁素体的:奥氏体(γ-Fe)在1147℃时碳溶解度最大(2.11 wt% C),是铁素体的近100倍,需明确区分两相
- 忽略“平衡状态”:题目隐含“平衡冷却(equilibrium cooling)”条件,非平衡冷却(如淬火)可能导致碳过饱和,但“最大溶解度”特指平衡状态下的数值(文档Week 3 Task 1强调“equilibrium cooling”的重要性)
Question 20
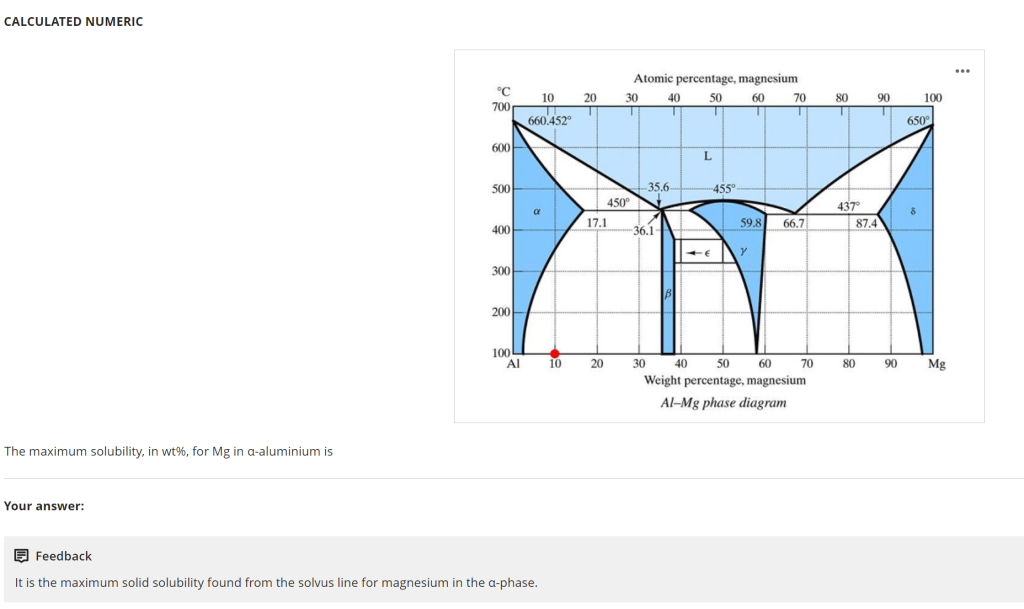
题目核心结论
镁(Magnesium, Mg)在α-铝(α-aluminium, α-Al,面心立方fcc固溶体)中的最大溶解度(maximum solubility)为 35.6 wt%(重量百分比)。
一、关键概念定义(带英文标注+文档位置)
1. 核心术语解析
| 中文术语 | 英文学术名词 | 定义(基于文档+相图分析) | 文档对应位置 |
|---|---|---|---|
| α-铝 | α-Aluminium (α-Al) | 镁在铝中的置换型固溶体(substitutional solid solution),晶体结构为面心立方(face-centered cubic, fcc),是Al-Mg系统低温下的稳定固相。 | Week 3 文档(2710 Week 3.pdf)Task 1“Binary Eutectic Phase Diagram”,e-book pages 44-55(固溶体定义) |
| 最大溶解度 | Maximum Solubility | 平衡状态下,溶质(Mg)能溶解在溶剂(α-Al)中的最高重量百分比,对应相图中α相区的固相线(solvus line)最高点。 | Week 1 文档(2710 Week 1.pdf)Task 1“Solubility limit”,e-book pages 1-8(溶解度极限定义) |
| 固相线 | Solvus Line | 相图中划分α单相区与α+第二相(如δ相、液相L)的曲线,曲线上每个点对应某温度下溶质的最大溶解度。 | Week 3 文档 Task 1“Solvus line”标注,e-book pages 44-55(Pb-Sn相图固相线示例) |
| α相区 | α-Phase Field | Al-Mg相图中以α-Al为单一相的区域,位于相图左下方,边界由固相线和液相线(liquidus line)界定。 | 图片中Al-Mg相图左侧标注“α”的区域,文档Week 3 Task 1“Phase Field”概念,e-book pages 44-55 |
2. 核心逻辑:为什么是35.6 wt%?
- α-Al的fcc晶格能容纳一定量的Mg原子(Mg原子半径与Al接近,形成置换固溶体)
- 相图中α相区的“固相线最高点”对应最大溶解度:该点是α相区与液相(L)或中间相(如δ相)的交界点,温度约455℃,此时Mg在α-Al中的溶解量达到峰值
- 超过35.6 wt% Mg时,冷却过程中会优先析出第二相(如δ相),不再形成单一α固溶体
二、相图中的定位与推导(结合图片+文档)
1. 图片相图的关键信息
- 横坐标:Weight percentage, magnesium(镁的重量百分比),标注有“35.6”数值
- 纵坐标:Temperature(温度),35.6 wt% Mg对应的温度约455℃
- 相区分布:35.6 wt% Mg是α相区的最大成分点,超过该成分后,相图进入“α+δ”或“L+α”双相区,说明Mg无法再更多溶解在α-Al中
2. 文档中的理论支持
- 固相线的物理意义:Week 3 文档 Task 1明确,固相线(solvus line)表示“溶质在溶剂中的最大溶解极限”,超过该浓度会析出第二相(如渗碳体、δ相),与feedback提示一致(“maximum solid solubility found from the solvus line”)
- 二元相图分析方法:Week 3 文档 Task 1“Lever Rule”部分提到,单相区的成分范围由相图边界界定,α相区的最大成分即为溶质的最大溶解度(e-book pages 44-55)
三、文档精确位置索引(立刻对照原文)
- 固溶体与溶解度极限定义:Week 1 文档(2710 Week 1.pdf)Task 1“Solubility limit”,e-book pages 1-8(以糖水、蜂蜜为例,说明溶解度上限由相图固相线决定)
- 二元相图固相线的意义:Week 3 文档(2710 Week 3.pdf)Task 1“Binary Eutectic Phase Diagram”,e-book pages 44-55(Pb-Sn相图中固相线标注,明确其为最大溶解度曲线)
- 单相区成分范围判断:Week 3 文档 Task 1“Phase Field”概念,e-book pages 44-55(单相区的边界对应成分极限)
四、易错点警示(考试高频丢分点)
- 混淆“重量百分比(wt%)”与“原子百分比(at%)”:题目明确要求wt%,图片中横坐标已标注“Weight percentage”,35.6是wt%数值,切勿误填原子百分比(Mg的原子百分比最大约20 at%);
- 误将液相线当作固相线:液相线(liquidus line)是“开始凝固的温度线”,固相线(solvus line)才是“最大溶解度线”,两者不可混淆(文档Week 3 Task 1“Liquidus vs Solvus”对比,e-book pages 44-55);
- 忽略平衡状态前提:最大溶解度是“平衡冷却(equilibrium cooling)”下的数值,非平衡冷却(如淬火)可能形成过饱和固溶体,但题目默认平衡状态(文档Week 3 Task 1强调“equilibrium cooling”的重要性)
0 条评论